マウスTCRα/β V(D)J可変領域の完全長シーケンスが可能
- イルミナ社次世代シーケンサー(MiSeq推奨)用ライブラリー作製キット
- TCR mRNAの完全長V(D)J可変領域のシーケンスが可能
- TCRα鎖、TCRβ鎖を同時または個別にライブラリー作製可能
- マルチプレックスPCRに依らない増幅でバイアスを低減
製品説明
SMARTer Mouse TCR a/b Profiling Kitは、イルミナ社次世代シーケンサーを用いたマウスT細胞受容体(TCR)のレパトア解析用ライブラリー作製キットである。マウスの脾臓、胸腺、末梢血単核細胞由来total RNA(10~500 ng)、あるいは精製済みT細胞1,000~10,000個から直接ライブラリーが作製でき、5’RACE法の応用によってTCR mRNAの完全長V(D)J 可変領域の配列を得ることができる。
TCRα鎖とTCRβ鎖のレパトアデータの取得を同一ライブラリーで、あるいは個別にライブラリーを作製して実施することが可能である。
マルチプレックスPCR法とは異なり、本キットではTCRα鎖、β鎖、それぞれに対して単一のプライマーを用いた2段階のPCRでライブラリー増幅を行っており、プライマーダイマー形成を抑えた高効率な増幅が可能である。
また、マルチプレックスPCRではプライマーに起因する配列特異的なバイアスが避けられないが、本製品は定常(非可変)領域にアニーリングする単一プライマーで全ての可変領域を増幅するため、プライマーに起因するバイアスが少ない。
本製品は5’RACE法を応用したSMARTテクノロジー(Switching Mechanism at 5’End of RNA Template)とLNAテクノロジーの利用により、高感度でバイアスの少ないレパトア解析が可能となっている。
4時間でインデックスを付加したライブラリー作製ができ、そのままイルミナ社次世代シーケンサーに用いてレパトア解析ができる。
TCRα鎖とTCRβ鎖のレパトアデータの取得を同一ライブラリーで、あるいは個別にライブラリーを作製して実施することが可能である。
マルチプレックスPCR法とは異なり、本キットではTCRα鎖、β鎖、それぞれに対して単一のプライマーを用いた2段階のPCRでライブラリー増幅を行っており、プライマーダイマー形成を抑えた高効率な増幅が可能である。
また、マルチプレックスPCRではプライマーに起因する配列特異的なバイアスが避けられないが、本製品は定常(非可変)領域にアニーリングする単一プライマーで全ての可変領域を増幅するため、プライマーに起因するバイアスが少ない。
本製品は5’RACE法を応用したSMARTテクノロジー(Switching Mechanism at 5’End of RNA Template)とLNAテクノロジーの利用により、高感度でバイアスの少ないレパトア解析が可能となっている。
4時間でインデックスを付加したライブラリー作製ができ、そのままイルミナ社次世代シーケンサーに用いてレパトア解析ができる。
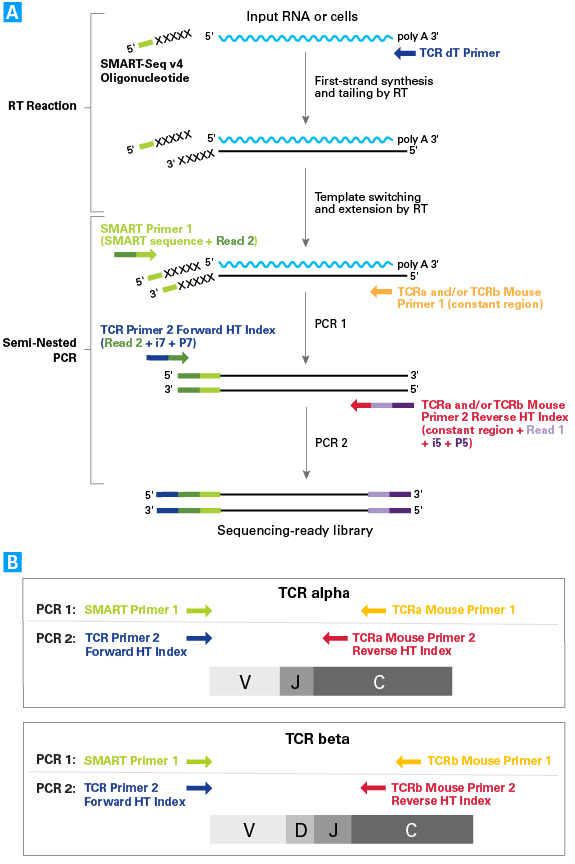
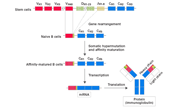
図1. SMARTer Mouse TCR a/b Profiling Kitを用いたライブラリー作製の概要
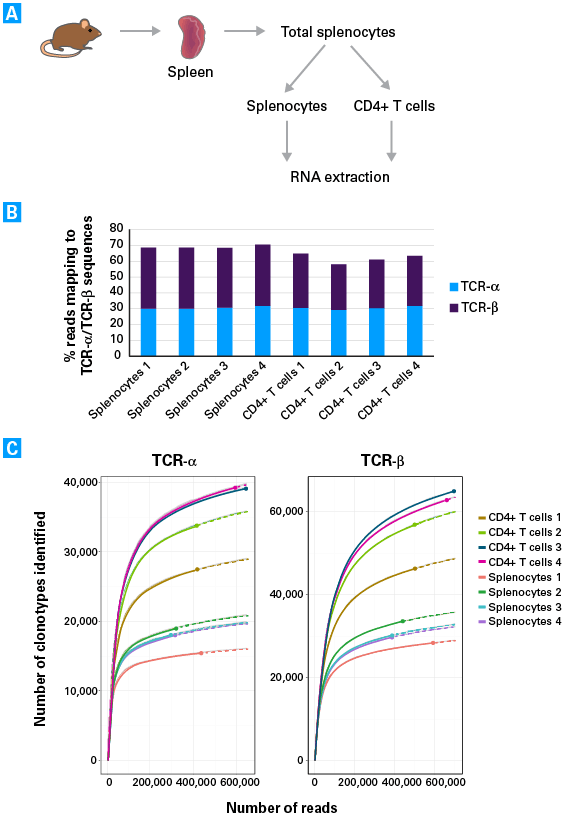
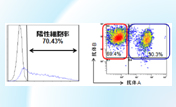
図2. SMARTer Mouse TCR a/b Profiling Kitを用いたマウス脾臓TCRの多様性評価
脾臓全T細胞とCD4+T細胞のTCRの多様性を比較することを目的として、脾臓から全脾細胞を分離して2つのグループに分け、1つのグループはそのまま、もう1つのグループはCD4+T細胞の精製を行った後、total RNAを抽出して、10 ngを用いてライブラリー調製を行った(パネルA)。
パネルB:TCRα、またはTCRβのCDR3領域にマッピングされたシーケンスリードの割合。約70%のリードがTCRαまたはTCRβにマッピングされ、良好なオンターゲット率を示した。
パネルC:TCRα(左)、TCRβ(右)に同定されたクローンタイプ数とリード数の解析
曲線がフラットになり始めた点を検出されるクローンタイプ数の飽和点とし、リード数が増えた場合の理論上のクローンタイプ数を点線で示した。TCR多様性評価に必要なリード数は、脾全細胞では約100,000リード以上、CD4+T細胞では約400,000リード以上であることが示された。
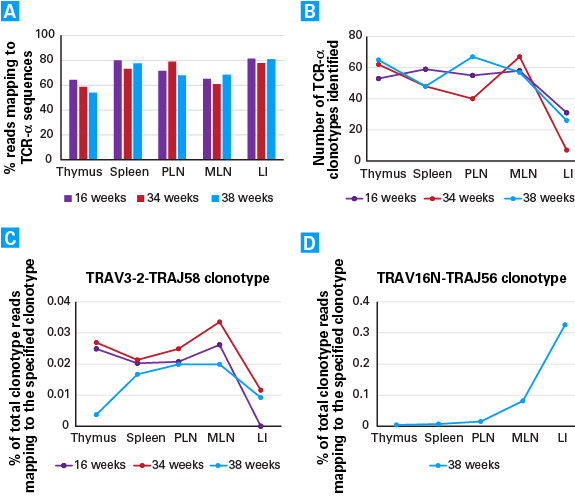
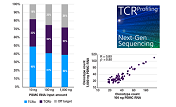
図3. トランスジェニックマウス各組織におけるTCRα 多様性の評価
<実験概要>
加齢に伴って大腸炎になるRag-1欠損マウスの各組織からtotal RNAを抽出後、本キットを用いてライブラリーを作製しNGS解析を行った。 16週齢、34週齢、38週齢のマウスの、胸腺(Thymus)、脾臓(Spleen)、末梢リンパ節(Peripheral Lymph Nodes, PLN)、腸間膜リンパ節(Mesenteric Lymph Nodes, MLN)、大腸(Large Intestine, LI)からtotal RNAを抽出後、10 ngを用いてライブラリーを調製した。但し、本実験ではTCRαをメインに検出するため、TCRα、TCRβに対する特異的プライマーの混合比率を1:1ではなく、2:1とした。シーケンスにはMiSeq(2×300 bp)を用いて、1サンプルあたり400,000リードで解析を行い、ソフトウェアはMiXCR(Bolotin et al. 2015)を使用した。
参考文献:Bolotin, D. A. et al. MiXCR: software for comprehensive adaptive immunity profiling. Nat. Methods12, 380–381 (2015).
<結果>
パネルA.各組織の各週齢において、シーケンスリードの約60~80%がTCRα CDR3領域にマッピングされ、高いオンターゲット率が得られた。
パネルB.同定されたTCRαクローン型の数は、各週齢のほとんどの組織で多かった一方、大腸(LI)では少ない結果となった。大腸で少なかった理由は、恐らくT細胞の浸潤が低いためと考えられる。
パネルC. TRAV3-2-TRAJ58クローン型の割合は、16週齢、34週齢のマウス胸腺では全体の約0.025%だったが、38週齢では約0.005%となった。一方、腸間膜リンパ節では週齢に関わらず高い割合を示したが、大腸では低い割合となった。このように発現量の少ないクローンでも、すべての組織において感度良く解析できた。
パネルD.38週齢のマウスではTRAV16N-TRAJ56クローン型が、大腸(LI)で非常に多く検出され、このクローンが大腸炎と関わりがあることが示唆された。
内容
SMARTer Mouse TCR a/b Profiling Kit Components
Package 1
Package 2
TCR a/b Mouse Indexing Primer Set HT for Illumina
Package 1
・Control RNA (1 μg/μl)
Package 2
・SMART-Seq v4 Oligonucleotide (48 μM)
・TCR dT Primer (12 μM)
・5X Ultra Low First-Strand Buffer
・SMARTScribe Reverse Transcriptase (100 U/μl)
・Nuclease-Free Water
・RNase Inhibitor (40 U/μl)
・10X Lysis Buffer
・Elution Buffer (10 mM Tris-HCl, pH 8.5)
・TCRa Mouse Primer 1 (12 μM)
・TCRb Mouse Primer 1 (12 μM)
・SMART Primer 1 (12 μM)
・PrimeSTAR GXL SP DNA Polymerase (1.25 U/μl)*
・5X PrimeSTAR GXL SP Buffer*
・dNTP Mixture (2.5 mM each)*
*96回用(製品コード 634404)では、Package3に入っています。
・TCR dT Primer (12 μM)
・5X Ultra Low First-Strand Buffer
・SMARTScribe Reverse Transcriptase (100 U/μl)
・Nuclease-Free Water
・RNase Inhibitor (40 U/μl)
・10X Lysis Buffer
・Elution Buffer (10 mM Tris-HCl, pH 8.5)
・TCRa Mouse Primer 1 (12 μM)
・TCRb Mouse Primer 1 (12 μM)
・SMART Primer 1 (12 μM)
・PrimeSTAR GXL SP DNA Polymerase (1.25 U/μl)*
・5X PrimeSTAR GXL SP Buffer*
・dNTP Mixture (2.5 mM each)*
*96回用(製品コード 634404)では、Package3に入っています。
TCR a/b Mouse Indexing Primer Set HT for Illumina
TCR a/b Mouse Indexing Primer Set HT for Illumina-12
TCR a/b Mouse Indexing Primer Set HT for Illumina-48
TCR a/b Mouse Indexing Primer Set HT for Illumina-96
・TCRa Mouse Primer 2 Reverse HT Index 1 (aR1; 12.5 μM)
・TCRb Mouse Primer 2 Reverse HT Index 1 (bR1; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 12回用(製品コード 634402)に添付
・TCRb Mouse Primer 2 Reverse HT Index 1 (bR1; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 12回用(製品コード 634402)に添付
TCR a/b Mouse Indexing Primer Set HT for Illumina-48
・TCRa Mouse Primer 2 Reverse HT Index 1~4 (aR1~aR4; 12.5 μM)
・TCRb Mouse Primer 2 Reverse HT Index 1~4 (bR1~bR4; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 48回用(製品コード 634403)に添付
・TCRb Mouse Primer 2 Reverse HT Index 1~4 (bR1~bR4; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 48回用(製品コード 634403)に添付
TCR a/b Mouse Indexing Primer Set HT for Illumina-96
・TCRa Mouse Primer 2 Reverse HT Index 1~8(aR1~aR8; 12.5 μM)
・TCRb Mouse Primer 2 Reverse HT Index 1~8 (bR1~bR8; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 96回用(製品コード 634404)に添付
・TCRb Mouse Primer 2 Reverse HT Index 1~8 (bR1~bR8; 12.5 μM)
・TCR Primer 2 Forward HT Index 1~12 (F1~F12; 12.5 μM)
・・・ 96回用(製品コード 634404)に添付
保存
SMARTer Mouse TCR a/b Profiling Kit Components
Package 1:-70℃
Package 2:-20℃
10X Lysis Buffer は融解後4℃保存
Elution Bufferは融解後室温保存
Package 3:-20℃
TCR a/b Mouse Indexing Primer Set HT for Illumina:-20℃
Package 1:-70℃
Package 2:-20℃
10X Lysis Buffer は融解後4℃保存
Elution Bufferは融解後室温保存
Package 3:-20℃
TCR a/b Mouse Indexing Primer Set HT for Illumina:-20℃
本製品以外に必要な試薬、機器(主なもの)
下記の製品は本キット中に含まれません。下記の製品はユーザーマニュアルに記載のProtocolで使用できることが確認されています。他製品では代替はできないため、ご注意ください。
SPRI Bead精製
その他
PCR増幅およびバリデーション
・First-Strand cDNA 合成専用のPCRサーマルサイクラー
・Double-Strand cDNA 増幅専用のPCRサーマルサイクラー
・High Sensitivity NGS Fragment Analysis Kit(Advanced Analytical社 Code DNF-474)
・DNA 1000 Kit(Agilent社 Code 5067-1504)
・Nuclease-free thin-wall PCR tube(0.2 ml;USA Scientific社 Code 1402-4700)
・Nuclease-free low adhesion 1.5 ml tube(USA Scientific社 Code 1415-2600)またはLoBind tube(Eppendorf社 Code.022431021)
・First-Strand cDNA 合成専用のPCRサーマルサイクラー
・Double-Strand cDNA 増幅専用のPCRサーマルサイクラー
・High Sensitivity NGS Fragment Analysis Kit(Advanced Analytical社 Code DNF-474)
・DNA 1000 Kit(Agilent社 Code 5067-1504)
・Nuclease-free thin-wall PCR tube(0.2 ml;USA Scientific社 Code 1402-4700)
・Nuclease-free low adhesion 1.5 ml tube(USA Scientific社 Code 1415-2600)またはLoBind tube(Eppendorf社 Code.022431021)
SPRI Bead精製
・Agencourt AMPure PCR Purification Kit(5 ml Beckman Coulter社 Code A63880、60 ml Beckman Coulter社 Code A63881)-増幅cDNAの精製に使用する
・Small volume用Magnetic stand
・100% Ethanol
・Small volume用Magnetic stand
・100% Ethanol
その他
・シングルチャンネルピペット: 10 μl、20 μlおよび200 μl
・8連チャンネルピペット: 20 μl、200 μl
・フィルターピペットチップ: 2 μl、20 μlおよび200 μl
・1.5 ml tube用minicentrifuge
・0.2 ml tubeまたはstrip用minicentrifuge
・8連チャンネルピペット: 20 μl、200 μl
・フィルターピペットチップ: 2 μl、20 μlおよび200 μl
・1.5 ml tube用minicentrifuge
・0.2 ml tubeまたはstrip用minicentrifuge
この製品を見た人は、
こんな製品も見ています
-

SMARTer Human TCR a/b Profiling Kit v2
UMI搭載!ヒトTCRα/β V(D)J可変領域の完全長シーケンスが可能
-

SMARTer® Human scTCR a/b Profiling Kit
シングルセルからのヒトTCRレパトア解析用キット
-

SMARTer® Human BCR IgG IgM H/K/L Profiling Kit
ヒトBCR H鎖/L鎖の可変領域の完全長シーケンス
-
T細胞レパトア解析(T細胞受容体多様性解析)
SMARTテクノロジー/5' RACE法とNGSの組み合わせによる網羅的なレパトア解析
-
SMARTer® Mouse BCR IgG H/K/L Profiling Kit
マウスIgG H鎖/L鎖の可変領域の完全長をシーケンス
-
SMARTer® Human TCR a/b Profiling Kit
ヒトTCRα/β V(D)J可変領域の完全長シーケンスが可能
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。