Standard Protocol
(TaKaRa One Step RNA PCR Kit (AMV))
■ 操作上の注意
本キットを使用する場合の注意事項です。使用前に必ずお読みください。
(1) 反応液は、Master mix(RNase Free dH2O、バッファー、dNTPmixture、MgCl2 等の混合液)を数回~10回分ぐらいまとめて調製すると便利です。Mastermixを作る ことにより、ピペッティングによるロスや、試薬の分注、撹拌回数が少なくなり、正確な試薬の分注を行うことができます。その結果、実験間のデータのばらつきも 防げます。
(2) Reverse Transcriptase, RNase Inhibitor, AMV-Optimized Taq等、酵素類の撹拌は泡立てないようにゆるやかに行ってください。また、ピペッティングの前に試薬を軽く遠心して、チューブの底に落としてください。
特に酵素類は、50%グリセロール溶液となっており粘度が高いため、注意深くゆっくりとピペッティングを行ってください。
(3) 酵素類は使用直前まで-20℃で保存し、使用後は直ちに-20℃に戻してください。
(4) Positive Control RNAは分解を防ぐためにできる限り凍結、融解は避けてください。少量ずつ分注後保存することをお勧めします。また、deep freezerをお持ちの場合は、-70~-80℃での保存をお勧めします。
(5) 試薬の分注を行うときは必ず新しいディスポーザブルチップを用い、サンプル間のコンタミネーションを極力防止してください。
(6)本キットによる逆転写反応は、特異的プライマーを用いて行います。Random primerやOligo dT primerは通常使用しません。
(1) 反応液は、Master mix(RNase Free dH2O、バッファー、dNTPmixture、MgCl2 等の混合液)を数回~10回分ぐらいまとめて調製すると便利です。Mastermixを作る ことにより、ピペッティングによるロスや、試薬の分注、撹拌回数が少なくなり、正確な試薬の分注を行うことができます。その結果、実験間のデータのばらつきも 防げます。
(2) Reverse Transcriptase, RNase Inhibitor, AMV-Optimized Taq等、酵素類の撹拌は泡立てないようにゆるやかに行ってください。また、ピペッティングの前に試薬を軽く遠心して、チューブの底に落としてください。
特に酵素類は、50%グリセロール溶液となっており粘度が高いため、注意深くゆっくりとピペッティングを行ってください。
(3) 酵素類は使用直前まで-20℃で保存し、使用後は直ちに-20℃に戻してください。
(4) Positive Control RNAは分解を防ぐためにできる限り凍結、融解は避けてください。少量ずつ分注後保存することをお勧めします。また、deep freezerをお持ちの場合は、-70~-80℃での保存をお勧めします。
(5) 試薬の分注を行うときは必ず新しいディスポーザブルチップを用い、サンプル間のコンタミネーションを極力防止してください。
(6)本キットによる逆転写反応は、特異的プライマーを用いて行います。Random primerやOligo dT primerは通常使用しません。
■ 各プライマーのシーケンス
| プライマー名 | シーケンス |
| Contorol F-1 primer | 5'-CTGCTCGCTTCGCTACTTGGA-3' |
| Contorol R-1 primer | 5'-CGGCACCTGTCCTACGAGTTG-3' |
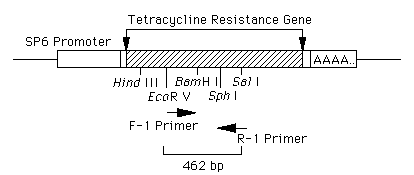
■ Positive Control RNA
本キットに添付されているPositive Control RNAは、SP6 Promoter領域下流にpBR322由来のテトラサイクリン耐性遺伝子を含む約1.4 kbpの断片を挿入したプラスミドpSPTet3を鋳型として、SP6 RNA Polymeraseを用いてin vitro transcriptionにより合成を行ったものである。
[器具]
実験器具に関しては、可能な限りディスポーザブルのプラスチック製品を使用してください。一般のガラス器具は以下の処理を行ってから使用してください。
(1)ガラス器具を0.1%ジエチルピロカーボネート(DEPC)溶液で、37℃、12時間処理する。
(2)残っているDEPCを除去するために、オートクレーブにかける。(120℃、30分)
RNA実験に用いる器具(プラスチックおよびガラス)は、他の器具と区別してRNA専用として用いることをお勧めします。
[溶液]
実験に用いる試薬溶液は、乾熱滅菌(180℃、60分)したガラス器具で調製し、用いる蒸留水は、0.1%DEPC処理を行いオートクレーブしてください。用いる溶液、蒸留水はすべてRNA実験専用としてお使いください。
[RNAサンプルの調製法]
RT-PCR法に用いるRNAサンプルは、通常少量のRNAがあればよい場合が多いので簡便な精製法が用いられることもありますが、できればGTC法(グアニジンチオシアネート法)等で高純度に精製したRNAを用いることをお勧めします。
組織、細胞からの抽出にはNucleoSpin RNA(製品コード 740955.50)やRNAiso Plus(製品コード 9108/9109)を用いると、短時間で高純度のtotal RNAを調製することができます。

■RNAサンプルの調製について
cDNA合成を成功させるためには純度の高いRNAサンプルを得ることが大切です。そのため、細胞内に含まれるRNaseの作用を抑えること、また使用する器具や溶液など外部からのRNaseの混入を避けることが大切です。RNA調製にあたっては、実験者の汗や唾液に含まれるRNaseの混入を防ぐため作業中は不必要に話さず、清潔なディスポーザブルグローブを着用し、RNA調製専用の実験台を設けるなどの細心の注意を払ってください。[器具]
実験器具に関しては、可能な限りディスポーザブルのプラスチック製品を使用してください。一般のガラス器具は以下の処理を行ってから使用してください。
(1)ガラス器具を0.1%ジエチルピロカーボネート(DEPC)溶液で、37℃、12時間処理する。
(2)残っているDEPCを除去するために、オートクレーブにかける。(120℃、30分)
RNA実験に用いる器具(プラスチックおよびガラス)は、他の器具と区別してRNA専用として用いることをお勧めします。
[溶液]
実験に用いる試薬溶液は、乾熱滅菌(180℃、60分)したガラス器具で調製し、用いる蒸留水は、0.1%DEPC処理を行いオートクレーブしてください。用いる溶液、蒸留水はすべてRNA実験専用としてお使いください。
[RNAサンプルの調製法]
RT-PCR法に用いるRNAサンプルは、通常少量のRNAがあればよい場合が多いので簡便な精製法が用いられることもありますが、できればGTC法(グアニジンチオシアネート法)等で高純度に精製したRNAを用いることをお勧めします。
組織、細胞からの抽出にはNucleoSpin RNA(製品コード 740955.50)やRNAiso Plus(製品コード 9108/9109)を用いると、短時間で高純度のtotal RNAを調製することができます。
■ 操作
一般的なRT-PCR例
- 下記に示す反応液を調製する。
1回の反応に用いるRNAサンプル量は、One Step RNA PCR Kitの場合、total RNAとして約1 μgの量が最適である。
試薬 使用量 最終濃度 [または反応系に加える量] 10×One Step RNA PCR Buffer 5 μl 1× 25 mM MgCl2 10 μl 5 mM 10 mM dNTP Mixture 5 μl 1 mM RNase Inhibitor(40 U/μl) 1 μl 0.8 U/μl AMV RTase XL(5 U/μl) 1 μl 0.1 U/μl AMV-Optimized Taq(5 U/μl) 1 μl 0.1 U/μl 上流specific primer*(20 μM) 1 μl 0.4 μM 下流 specific primer**(20 μM) 1 μl 0.4 μM Positive Control RNA 1 μl total RNAの場合約1 μg またはExperimental Sample*** RNase Free dH2O 24 μl 合計 50 μl
* Positive Control RNAの場合:Control F-1 Primer
** Positive Control RNAの場合:Control R-1 Primer
*** 発現量の少ないRNAの場合、25 μlまでサンプル量を増やせます。 - 反応液を混合後、ミネラルオイル50~100 μlまたは、AmpliWaxを重層する。(TaKaRa Thermal Cycler MPまたはPersonalの場合不要) 調製済みのチューブをサーマルサイクラーにセットし、次のプログラムで反応を行う。
一般的な反応条件〈Positive Control RNAの場合〉
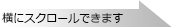
50℃〈50℃〉 30 min.〈15 min.〉 RT反応 94℃〈94℃〉 2 min.〈2 min.〉 RTaseの不活化 94℃〈94℃〉 30 sec.〈30 sec.〉 37~65℃〈60℃〉 30 sec.〈30 sec.〉 PCR反応:25~30 cycles〈28 cycles〉 72℃〈72℃〉 1~10 min.〈1.5 min.〉 - 反応終了後、反応液の一部(5~10 μl)をアガロースゲル電気泳動を行い、反応産物を確認する。PCR増幅産物は解析するまで凍結保存する。コントロール反応の場合、462 bpが検出される。
■ PCRの条件について
- アニーリング温度
コントロールRNAの場合、60℃で行っていますが、実際のサンプルの場合は条件が変わりますので、37~65℃の範囲で至適温度を調べてください。 - 伸長時間
伸長時間は、ターゲットの鎖長にあわせて設定します。通常、AMV-Optimized Taqは70~80℃で1分間に2,000~4,000 baseの割合でextensionを行います。 - Cycle数
cDNA量が少ない場合は、40~50 cyclesで行ってください。
