Smart Cycler® II System を用いる場合の操作方法
TB Green Premix DimerEraser (Perfect Real Time)(製品コード RR091A/B)
- 下記に示すPCR反応液を調製する。
1反応あたり 試薬 使用量 最終濃度 TB Green Premix DimerEraser(2×) 12.5 μl 1× PCR Forward Primer(10 μM) 0.75 μl 0.3 μM*1 PCR Reverse Primer(10 μM) 0.75 μl 0.3 μM*1 template(<100 ng) 2 μl *2 滅菌精製水 9 μl Total 25 μl *1 最終primer濃度は0.3 μMで良い結果が得られる場合が多いが、反応性に問題がある時は0.2~1.0 μMの範囲で最適な濃度を検討すると良い。
*2 template溶液中に存在するターゲットのコピー数により異なる。段階希釈して適当な添加量を検討する。DNA template 100 ng以下を用いることが望ましい。また、RT-PCRでcDNA(RT反応液)をtemplateとして添加する場合は、PCR反応液容量の10%以下になるようにする。
- 反応チューブをSmart Cycler用遠心機で軽く遠心後、Smart Cyclerにセットし、反応を開始する。
PCRは、下記の3 step PCRによる標準プロトコールで行うことをお勧めします。
反応性に問題がある場合には、下記の「PCR条件反応について」を参考に最適なPCR条件を検討してください。
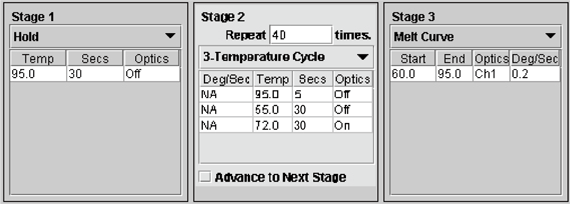
Stage 1:初期変性
Hold
95℃ 30秒
Stage 2:PCR反応
Repeat:40 times
95℃5秒
55℃ 30秒
72℃ 30秒
Stage 3:融解曲線分析 - 反応終了後、増幅曲線と融解曲線を確認し、定量を行う場合は検量線を作成する。
解析方法は、装置の取扱説明書をご参照ください。
※使用上の注意
本製品に使用しているTaKaRa Ex TaqHS はポリメラーゼ活性を抑制する抗Taq抗体を利用したホットスタートPCR用酵素です。他社の化学修飾タイプのホットスタートPCR酵素で必要なPCR反応前の95℃(5~)5分の活性化ステップは行わないでください。必要以上の熱処理を加えると酵素活性が低下し、増幅効率、定量精度に影響を及ぼす傾向があります。
PCR反応前に鋳型の初期変性を行う場合でも、通常95℃ 30秒で充分です。
PCR反応条件について
初期変性
初期変性は通常95℃、30秒で充分です。環状プラスミドやゲノムDNAなど変性しにくい鋳型でも、ほとんどの場合、この条件で良好に反応できます。鋳型の状態によっては、95℃、1~2分程度に延長することが可能ですが、時間が長すぎると酵素の失活を招く恐れがありますので、2分以上の条件は推奨しません。
PCR 条件と反応特異性
反応特異性を上げるには、アニーリング温度を上げるか2 step PCRに変更します。特に高分子側の非特異的増幅が見られる(融解曲線分析で目的のターゲットより高いTm値のピークが見られる)場合には、2 step PCRへの変更が有効です。
|
→ |
|
→ |
|
→ |
|
PCR条件と増幅効率
増幅効率を上げるには、伸長反応時間を延ばします。
|
→ |
|
