LightCycler®を用いる場合の操作方法
MightyAmp for Real Time (TB Green Plus)(製品コード R075A/B)
- 下記に示すPCR反応液を調製する。
<1反応あたり>
試薬 使用量 最終濃度 MightyAmp for Real Time(TB Green Plus)(2×) 10 μl 1× PCR Forward Primer (10 μM) 0.4 μl 0.2 μM*1 PCR Reverse Primer (10 μM) 0.4 μl 0.2 μM*1 template (<100 ng) 2 μl *2 滅菌水 7.2 μl Total 20 μl *1 最終primer濃度は0.2 μMで良い結果が得られる場合が多いが、反応性に問題がある時は0.1~1.0 μMの範囲で最適な濃度を検討すると良い。
*2 template溶液中に存在するターゲットのコピー数により異なる。段階希釈して適当な添加量を検討する。DNA template 100 ng以下を用いることが望ましい。また、RT-PCRでcDNA (RT反応液) をtemplateとして添加する場合は、PCR反応液容量の10%以下になるようにする。
- 反応を開始する。
PCRキャピラリーを遠心機で軽く遠心後、LightCyclerにセットし、反応を開始する。
* PCR反応は、下記の標準プロトコールで行うことをお勧めします。まずはこのプロトコールを試し、必要に応じてPCR反応条件を至適化する。PCR条件を至適化する場合は下記の「PCR条件について」を参照してください。
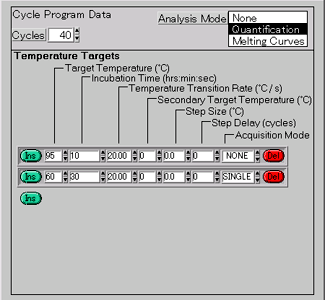 標準プロトコール
標準プロトコール
Stage 1:初期変性
98℃ 2分 20℃/秒
1サイクル
Stage 2:PCR反応
98℃ 10秒 20℃/秒
60℃ 15秒 20℃/秒
68℃ 1分/kb 20℃/秒
(500 bp以下は30秒)
40サイクル
Stage 3:融解曲線分析
95℃ 0秒 20℃/秒
65℃ 15秒 20℃/秒
95℃ 0秒 0.1℃/秒
※使用上の注意
本製品に使用しているMightyAmp DNA Polymeraseは強力なホットスタート抗体を使用しているので、必ず98℃、2分の初期変性を行い、抗体を熱変性させてください。 -
反応終了後、増幅曲線と融解曲線を確認し、定量を行う場合は検量線を作成する。
解析方法は、リアルタイムPCR装置の取扱説明書をご参照ください。
PCR条件について
【PCR条件の検討】○反応特異性を上げるには
アニーリング温度を上げると反応特異性が改善することがある。増幅効率とのバランスを確認しながら、検討してください。
アニーリング温度を上げると反応特異性が改善することがある。増幅効率とのバランスを確認しながら、検討してください。
標準プロトコール
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 60℃ | 15秒 | |
| 68℃ | 1分/kb |
→
アニーリング温度を上げる
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| ~64℃ | 15秒 | |
| 68℃ | 1分/kb |
→
シャトルPCRにする
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 68℃ | 1分/kb |
○増幅効率を上げるには
伸長時間を延ばすか、アニーリング温度を下げることにより、増幅効率が改善することがある。以下の手順で検討してください。
伸長時間を延ばすか、アニーリング温度を下げることにより、増幅効率が改善することがある。以下の手順で検討してください。
標準プロトコール
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 60℃ | 15秒 | |
| 68℃ | 1分/kb |
→
伸長時間を延ばす
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 60℃ | 15秒 | |
| 68℃ | ~2分/kb |
→
アニーリング温度を下げる
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 55℃ | 15秒 | |
| 68℃ | ~1分/kb |
→
伸長時間を延ばす
| 98℃ | 2分 | |
| 98℃ | 10秒 | |
| 55℃ | 15秒 | |
| 68℃ | ~2分/kb |
