ラット骨抽出物のウェスタンブロッティング
本抗体は、大腸菌で発現させたラットDMP1タンパク質に反応し、かつラット骨抽出液中の天然型DMP1タンパク質に反応することが確認されている。3)
ここでは、ラットの頭蓋骨EDTA抽出物について、本ペプチド抗体を用いてウェスタンブロッティングを行った例を示す。
ここでは、ラットの頭蓋骨EDTA抽出物について、本ペプチド抗体を用いてウェスタンブロッティングを行った例を示す。
- 【方法】
- (1)骨抽出物の調製
1. 24日齢SDラット(雌)、70個体の頭蓋骨から可能な限り丁寧に結合組織を除き、頭蓋骨をPBSで洗浄して回収した(収量20 g)。 2. 約1 Lの液体窒素中で、すり鉢棒により粉砕後、直ちに100 mlの0.5 M EDTA・2Na含有抽出液を加え、4℃で72時間抽出を行った。 [抽出液の組成]
0.5 M EDTA・2Na
5 mM ベンザミジン
30 μM PMSF
10 mM アミノカプロン酸
1 μg/ml ロイペプチン
20 mM Tris-HCl (pH7.8)3. 抽出物を遠心 (9,000 rpm) し、その上清を5 Lの純水に対して、2日間かけて計4回透析した。 4. 透析した液 (約100 ml) を-80℃で保存し、その一部をウェスタンブロットアッセイのサンプルとした。 - (2)ウェスタンブロッティング
免疫前のウサギ血清 (コントロール) 、精製前の抗DMP1ペプチド抗血清、プロテインA精製抗体、アフィニティー精製抗体 (本製品) 、およびウサギ精製IgG (コントロール) をそれぞれ用いて行い、結果を比較した。1. サンプルを還元・過熱処理した後、5~20%SDSグラジエントゲルの各レーンに10 μlずつアプライし、常法に従ってSDS-PAGEを行った。 2. 電気泳動後、ゲル上のタンパク質をPVDF膜にトランスファーした。 3. ブロックエース (原液) でブロッキングした後、PVDF膜をレーンごとに切り、以下の溶液にそれぞれ浸して室温で1時間反応させた。 A:免疫前のウサギ血清 (1,000倍希釈液)
B:精製前の抗DMP1ペプチド抗血清 (1,000倍希釈液)
C:プロテインA精製抗体 (10 μg/ml)
D:アフィニティー精製抗体 (10 μg/ml)
E:ウサギ精製IgG (10 μg/ml)4. 0.1% Tween含有PBSで振とう洗浄した後、ウサギIgG-POD標識抗体 (ICN)の500倍希釈液に膜を浸し、室温で1時間反応した。
再び、0.1% Tween含有PBSで振とう洗浄した後、発色基質TrueBlueにより発色させた。 - 【結果】
- 精製前の抗血清および精製抗体を用いた場合で、分子量23,000付近に明瞭なバンドが観察された。しかし、検出されたバンドは理論サイズよりもかなり小さいため、骨抽出物の精製過程でDMP1タンパク質の分解が起こったものと考えられる。
抗体の特異性は、精製が進むにつれて向上していくことが確認された。プロテインA精製抗体の場合では、低分子の位置に非特異的と思われるバンドが認められたが、アフィニティー精製抗体 (本製品) の場合では、バンドは単一であった。
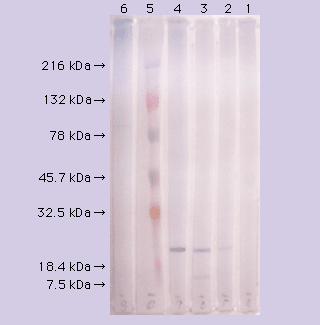
レーン
1:免疫前のウサギ血清 (×1,000)
2:精製前の抗DMP1ペプチド抗血清 (×1,000)
3:プロテインA精製抗体 (10 μg/ml)
4:アフィニティー精製抗体 (本製品)(10 μg/ml)
5:コントロールウサギ精製IgG (10 μg/ml)
