SCDaseを用いた2層系によるリゾスフィンゴ脂質の高効率生産
SCDaseは各種スフィンゴ脂質を特異的に加水分解し、そのリゾ体と脂肪酸を生成する。さらにSCDaseは、リゾ体と脂肪酸からスフィンゴ脂質を生成する加水分解の逆反応、およびスフィンゴ脂質の脂肪酸を交換する反応を効率良く行う(製品説明 参照)。
加水分解反応を行わせる際、特定の有機溶媒を添加すると、水層から脂肪酸が除去されて逆反応が抑えられるため、リゾ体の収率を上げることができる。小スケールおよび大スケールにおける、この2層系での加水分解の実際の操作と注意点をそれぞれ図1および図2に示す。
2層系で使用できる有機溶媒(図1, 2の*1)はいくつかあるが、反応促進効率が高く、不活性で使用しやすい脂肪族炭化水素が勧められる。この場合、溶媒の炭素数が多いほど、基質の加水分解率が高くなる。
しかし、炭素数が多いほど、融点および沸点が上がり、反応終了後の取扱いが難しくなる。通常は、n-デカンを使用するのが便利である。有機溶媒としてn-デカンを用いた場合の各種基質の分解率は以下の通りである(図1の*2の条件下)。
有機溶媒の除去(図1, 2の*3)の方法は、使用する有機溶媒の性質によって少し異なる。n-デカンを用いた場合では、ピペット等でできるだけ除いた後、減圧濃縮することにより完全に除去することができる。n-ヘプタデカンのように炭素数の大きいものは、室温で固定するため減圧濃縮が困難である。このような溶媒を用いた場合は、ピペット等でできるだけ除いた後、n-デカンやクロロホルムのような揮発性の溶媒で洗浄し、そのあと減圧濃縮することにより除くことが可能である。この時、リゾ体が洗浄溶媒に移らないことを確認する必要がある。得られたリゾ体の精製(図1, 2の*4)は、TLCや逆相クロマトグラフィーによって行うことができる。
加水分解反応を行わせる際、特定の有機溶媒を添加すると、水層から脂肪酸が除去されて逆反応が抑えられるため、リゾ体の収率を上げることができる。小スケールおよび大スケールにおける、この2層系での加水分解の実際の操作と注意点をそれぞれ図1および図2に示す。
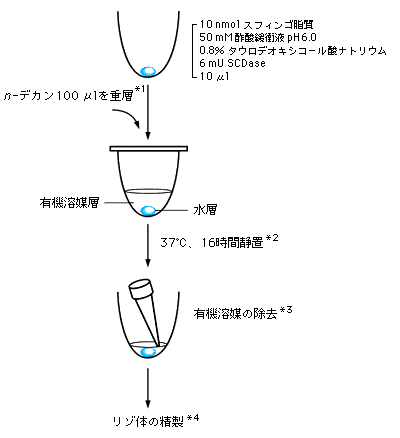
図1 小スケールでの各種スフィンゴ脂質の加水分解
*1~4:下記参照。
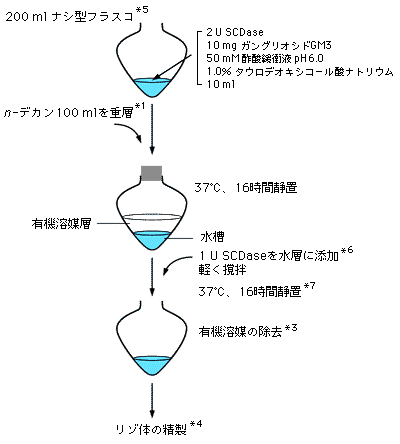
図2 大スケールでのガングリオシドGM3の加水分解
*1~4 : 下記参照。 *5 : 反応容器にガラス容器を使用する場合は、前もってシリコナイズ処理をしておいてください。表面処理をしていないガラス容器を用いると、リゾ体の収率が大きく低下する場合があります。 *6 : 16時間反応後、反応液の一部を取って加水分解反応の進行具合をTLC等で確認します。未反応物が多い場合、SCDaseを追加することにより収率を高めることができます。 *7 : 加水分解率 95%(GM3を基質とした場合)
2層系で使用できる有機溶媒(図1, 2の*1)はいくつかあるが、反応促進効率が高く、不活性で使用しやすい脂肪族炭化水素が勧められる。この場合、溶媒の炭素数が多いほど、基質の加水分解率が高くなる。
溶 媒 分解率(%) n-デカン 95 n-ドデカン 95 n-ペンタデカン 97 n-ヘプタデカン 97 n-オクタデカン 97 (GM1を基質として使用し、小スケールで反応を行った場合)
しかし、炭素数が多いほど、融点および沸点が上がり、反応終了後の取扱いが難しくなる。通常は、n-デカンを使用するのが便利である。有機溶媒としてn-デカンを用いた場合の各種基質の分解率は以下の通りである(図1の*2の条件下)。
基 質 分解率(%) Gal-Cer 82 Sulfatide 93 GM1 96 GM3 97 GD1a 95 GT1b 71 Asialo・GM1 93 Sphingomyelin 48
有機溶媒の除去(図1, 2の*3)の方法は、使用する有機溶媒の性質によって少し異なる。n-デカンを用いた場合では、ピペット等でできるだけ除いた後、減圧濃縮することにより完全に除去することができる。n-ヘプタデカンのように炭素数の大きいものは、室温で固定するため減圧濃縮が困難である。このような溶媒を用いた場合は、ピペット等でできるだけ除いた後、n-デカンやクロロホルムのような揮発性の溶媒で洗浄し、そのあと減圧濃縮することにより除くことが可能である。この時、リゾ体が洗浄溶媒に移らないことを確認する必要がある。得られたリゾ体の精製(図1, 2の*4)は、TLCや逆相クロマトグラフィーによって行うことができる。