操作
操作の流れ
1.サンプルの調製
3.反応液の調製と反応開始
Viable Bacteria Selection Kit for PCRシリーズによるEMA処理を行い、NucleoSpin Tissue XS等を用いてDNAを抽出する。
2.qPCR/PCR装置のセッティング3.反応液の調製と反応開始
反応液を調製する
↓
反応液を反応チューブに分注し、滅菌精製水(陰性コントロール)、または検体サンプル、またはPositive Controlを添加する
↓
反応チューブをqPCR/PCR装置にセットし反応を開始する
↓
4.検出↓
反応液を反応チューブに分注し、滅菌精製水(陰性コントロール)、または検体サンプル、またはPositive Controlを添加する
↓
反応チューブをqPCR/PCR装置にセットし反応を開始する
↓
| 【リアルタイムPCR】 画面上にリアルタイムで増幅曲線が表示される ↓ 反応終了 ↓ 判定 |
【エンドポイントPCR】 反応終了 ↓ アガロースゲル電気泳動で確認 ↓ 判定 |
1.サンプルの調製(エリア2で実施)
検体の懸濁液を用意し、Viable Bacteria Selection Kit for PCRシリーズによるEMA処理を行った後、NucleoSpin Tissue XS等によるDNA抽出を行う(操作方法の詳細は各製品の取扱説明書を参照)。
2.反応液の調製(リアルタイムPCR、エンドポイントPCR で共通)
コントロール反応について
本キットでは、Viable Bacteria Selection Kit for PCRシリーズの試薬コンポーネントに添加されているプラスミドDNAをqPCR/PCRで増幅するが、Viable Bacteria Selection Kit for PCRシリーズによるEMA処理が正しく行われると増幅産物が検出されない。
PCR反応自体の成否を確認するために、必ずPositive Controlを用いた陽性コントロール反応を同時に行う。また、コンタミネーションの有無を確認するためにサンプルのかわりに滅菌精製水を加える陰性コントロール反応も同時に行うことを推奨する。
| (1) | 下記に示す反応液を氷上で調製する。 鋳型(検体サンプル等)以外のコンポーネントを必要本数+α分調製し、反応チューブに20 μlずつ分注後、軽くふたをする。必要本数として、サンプル数+ 2本(Positive Control、陰性コントロールとして滅菌精製水を加えるもの)を準備する。 |
| 液量(1反応) | 最終濃度 | |
| 2×Cycleave Reaction Mixture | 12.5 μl | 1× |
| Primer/Probe Mix(5×conc.) | 5 μl | 1× |
| 検体サンプルor Positive Control or 滅菌精製水 | (5 μl)* | |
| dH2O | 2.5 μl | |
| total | 25 μl | |
| * 検体サンプル等の鋳型は、この段階では加えない | ||
| (2) | 陰性コントロールとして、サンプルの代わりに滅菌精製水を加えたものを1本調製し、しっかりふたをする。 | ||
| (3) | サンプル(鋳型)の添加 (1)で分注した残りのチューブについて、サンプルまたはPositive Controlを調製液に添加し、しっかりふたをする。
|
||
| (4) | 0.2 mlチューブ用の卓上遠心機で軽く遠心を行い、qPCR/PCR装置にセットする。 【注意】 反応液調製後、なるべく1時間以内に反応を開始する。 |
3.qPCR/PCR反応と結果の解析
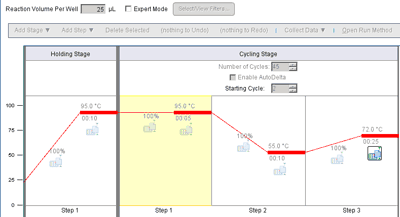
| ■ | リアルタイムPCR (1) 以下の条件でリアルタイムPCRを行う。
陰性コントロール反応および陽性コントロール反応での増幅曲線を確認する。 陰性コントロールにおいて蛍光シグナル変化の無いベースラインが得られ、閾値を超えていないことを確認する。陽性コントロールにおいて増幅曲線が描かれ、閾値を超えていることを確認する。 検体サンプルのベースラインや増幅曲線が正常に描かれていることを確認する。 ◆判定結果について
|
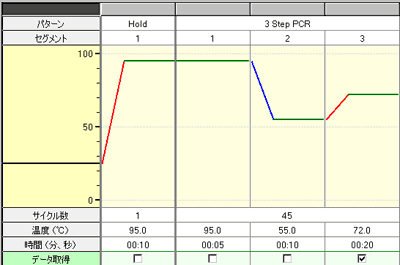
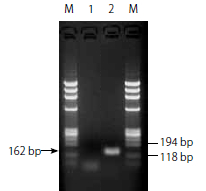
| ■ | エンドポイントPCR 反応終了後アガロースゲル電気泳動を行い、目的サイズ(162 bp)のバンドを検出することで判定を行う。 (1) 以下の条件でPCR増幅を行う。
◆結果判定について
|
|||||||||||||||||||||||||||||