アデノ随伴ウイルスベクターを用いた各種組織由来ヒト間葉系幹細胞への遺伝子導入
アデノ随伴ウイルス(Adeno-associated Virus: AAV)ベクターを用いた遺伝子導入は、安全性や取り扱いのし易さから研究分野から遺伝子治療などの医療分野まで広く使用されている。しかし複数のセロタイプが存在し、それぞれに組織指向性が異なるため、標的とする細胞に合せて最適な血清型のAAVを選択する必要がある。今回、蛍光タンパク質であるZsGreen1を発現する4種類の血清型のAAV(AAV1、2、5、6)を使用し、フローサイトメトリー(Flow cytometry: FCM)解析にて3種類の組織由来ヒト間葉系幹細胞(Human Mesenchymal Stem Cells: hMSC)への遺伝子導入効率を評価した。
アデノ随伴ウイルス(AAV)ベクター作製受託はこちら
- 実験方法:
- <ZsGreen1発現AAVベクターの作製>
AAVpro Helper Free System(製品コード 6673、6230、6650、6651)、pAAV-ZsGreen1 Vector(製品コード 6231)を用い、本製品の標準プロトコールに従い、AAV-ZsGreen1ウイルスベクターを作製した。 - <AAV-ZsGreen1ベクターの抽出、精製>
AAVpro Purification Maxi (All Serotypes)(製品コード 6666)を用い、本製品の標準プロトコールに従い、AAV-ZsGreen1ベクターの精製を行った。 - <hMSCへの感染>
3種類のhMSC- ヒト脂肪組織由来間葉系幹細胞(hMSC from Adipose Tissue: hMSC-AT)
- ヒト骨髄由来間葉系幹細胞(hMSC from Bone Marrow: hMSC-BM)
- ヒト臍帯マトリックス由来間葉系幹細胞(hMSC from Umbilical Cord Matrix: hMSC-UC)
培地
Cellartis MSC Xeno-Free Culture Medium(製品コード Y50200)
Day0 6 wellプレートに、各種組織由来hMSCを4×104 cells播種した。
Day1 培地交換を行い、各血清型のAAVをMOI=100,000となるように添加し、各組織由来のhMSCに感染させた。 - <発現強度の解析>
hMSC-ATとhMSC-BMに関しては72時間後、hMSC-UCは48時間後に細胞を剥離し、FCMで解析を行った。 - 結果:
-
今回の検討に使用した全ての組織由来hMSCにおいて、血清型6のAAVベクターによる遺伝子導入効率がもっとも高かった。
- hMSC-AT
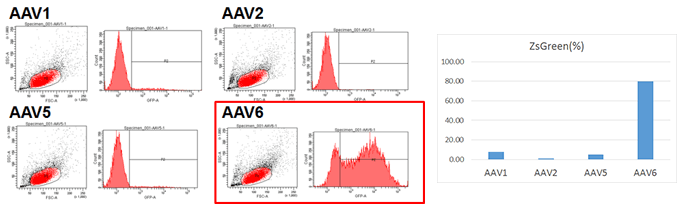
- hMSC-BM
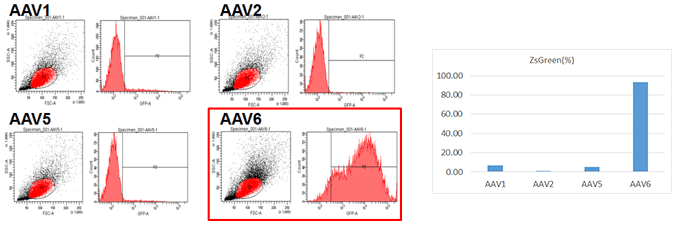
- hMSC-UC
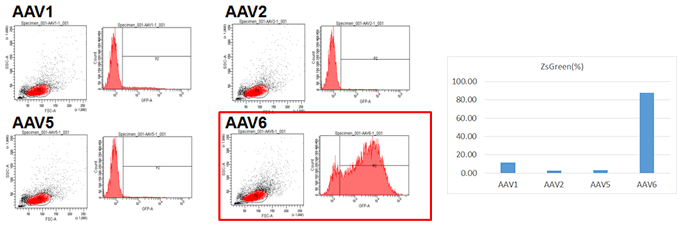
- hMSC-AT
アデノ随伴ウイルス(AAV)ベクター作製受託はこちら
