“CereAAV™”を用いたマウス脳への遺伝子導入
アデノ随伴ウイルス(Adeno-associated Virus:AAV)ベクターを用いた遺伝子導入は、安全性や取り扱いのしやすさから研究分野をはじめ遺伝子治療などの医療分野まで広く使用されています。AAVベクターを使用した脳を標的とする遺伝子治療では、静脈注射により全身投与した場合に、脳以外の臓器(肝臓等)にも蓄積する傾向があり、副作用の原因となる可能性が指摘されています。このため、脳疾患を対象とした遺伝子治療には、脳指向性の高いAAVベクターが求められています。
タカラバイオでは脳指向性を高めることを目的とし、AAV2をベースに遺伝子工学的改変と独自スクリーニング技術によりCereAAVを開発しました。今回、AcGFPを発現する各種血清型AAVベクター(CereAAV, AAV2, AAV9)を作製し、マウスへ尾静脈投与による脳指向性を比較しました。
静脈投与用 精製AAVベクターの調製
293T細胞へ各種プラスミドベクター*を共導入し、細胞と培養上清からAAVベクターを抽出。次に抽出液をクロマトグラフィー処理によりAAVベクターを精製し、さらに超遠心処理を経てfull particleのAAVベクターを回収後、溶媒を最終調製バッファーに置換したものを精製AAVベクターとした。これらの操作は各種血清型ごとに実施し、得られた精製AAVベクターをマウスへの尾静脈投与に使用した。
*各種血清型に応じてpRCは変更
AAVベクターのマウスへの尾静脈投与
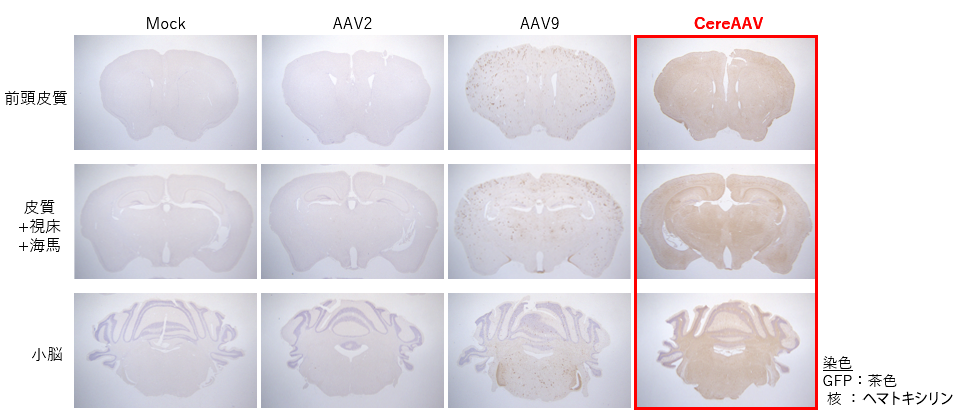
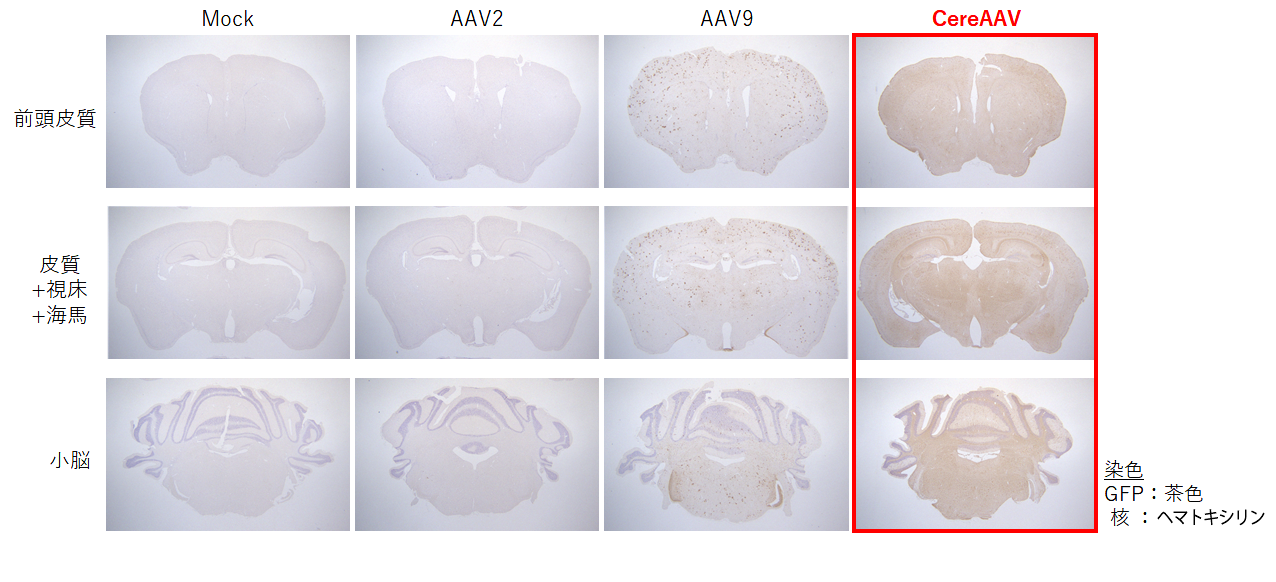
各AAVベクター(CereAAV, AAV2, AAV9)を8週齢のBALB/cマウスに対し、1×1012 vg/マウスで尾静脈投与し、4週間後に麻酔下で灌流固定後、脳を摘出し、パラフィン包埋を行った。切片を作製し、一次抗体として抗GFP抗体で処理後、DAB染色およびヘマトキシリン染色を行い、脳指向性について評価した。
脳への指向性が比較的高いと言われているAAV9において脳の各部位でAcGFPの発現が見られたが、CereAAVではAAV9よりはるかに多くの染色が確認された。