わずか4時間で組換えレトロウイルスのRNAタイターを測定
- わずか4時間で組換えレトロウイルスのRNAタイターを測定
- 同日中にウイルス回収~タイター測定および感染が可能
- MMLVベースのレトロウイルスベクターに使用可能(※MSCVベースのレトロウイルスには使用不可)
- 正確なタイターを得ることができるので安定した感染実験が可能
Retro-X qRT-PCR Titration Kitを用いると組換えレトロウイルスの力価(RNAタイター)を極めて迅速、簡便かつ正確に測定できる。RNAの簡易精製を行った後、One-Step qRT-PCRとインターカレーター法を組み合わせて、添付の校正用RNAを用いて作成した検量線からレトロウイルスゲノム量を測定する(図1)。
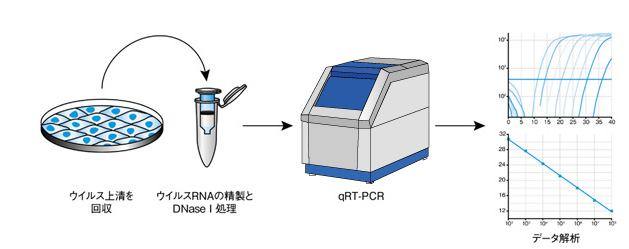
図1. Retro-X qRT-PCR Titration Kitの操作手順
このような長時間を要する力価測定法では、凍結解凍の繰り返しや長期のウイルス保管を余儀なくされ、その間にウイルスストックの感染性が低下してしまう。しかし、その低下の程度は測定できない。多くの場合、何日も経った推定力価をやむなく感染性とMOIの算出に使用することになる。
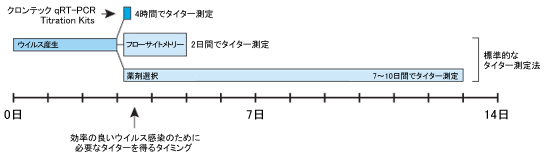
図2. Retro-X qRT-PCR Titration Kitは非常に短時間で力価測定可能
標準的な形質導入による力価測定法は、終了までに最長10日間を要する。一方、Retro-X qRT-PCR Titration Kitの所要時間はわずか4時間で、ウイルスの回収、力価測定、および標的細胞への感染全てを同日中に実施できる。
一方、ClontechのqRT-PCRタイター測定法ではわずか4時間で結果が得られる。qRT-PCR法を用いることでタイター測定に要する時間、すなわちウイルス回収後、感染を行うまでのインターバルを短縮でき、ウイルス回収を行ったその日のうちに感染までを行うことが可能になる。力価測定に時間を要してウイルス力価の低下を招くことがなくなるため、意図した通りのMOIで感染を行い再現性の高い結果を得ることができる。
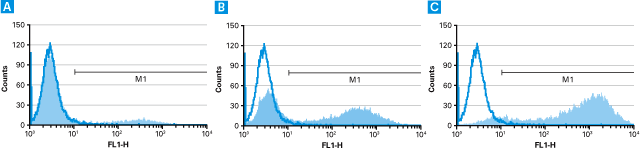
図3. タンパク質発現はMOIが高くなるほど増加する
様々な濃度のアンホトロピックレトロウイルスを含む上清で形質導入し、ZsGreen1蛍光タンパク質を発現させたNIH 3T3細胞のヒストグラム。ウイルス量の増加により感染細胞数およびZsGreen1の発現レベルが増加する。パネルA~C:MOI 0.3、3、および30での感染の結果。それぞれ8%、50%、および97%のZsGreen1陽性細胞(蛍光強度>10)が得られた(M1期細胞)。

図1. Retro-X qRT-PCR Titration Kitの操作手順
短時間のRNAタイター測定により再現性の高い感染実験が可能
感染性を基にした標準的な力価測定法には、蛍光マーカー、薬剤耐性、または細胞染色を用いた方法があるが、終了までに2~10日間を要する。(図2)。これらの中で、最も迅速なフローサイトメトリーによる測定でさえ、48時間未満では力価を正確に得ることができない。このような長時間を要する力価測定法では、凍結解凍の繰り返しや長期のウイルス保管を余儀なくされ、その間にウイルスストックの感染性が低下してしまう。しかし、その低下の程度は測定できない。多くの場合、何日も経った推定力価をやむなく感染性とMOIの算出に使用することになる。

図2. Retro-X qRT-PCR Titration Kitは非常に短時間で力価測定可能
標準的な形質導入による力価測定法は、終了までに最長10日間を要する。一方、Retro-X qRT-PCR Titration Kitの所要時間はわずか4時間で、ウイルスの回収、力価測定、および標的細胞への感染全てを同日中に実施できる。
一方、ClontechのqRT-PCRタイター測定法ではわずか4時間で結果が得られる。qRT-PCR法を用いることでタイター測定に要する時間、すなわちウイルス回収後、感染を行うまでのインターバルを短縮でき、ウイルス回収を行ったその日のうちに感染までを行うことが可能になる。力価測定に時間を要してウイルス力価の低下を招くことがなくなるため、意図した通りのMOIで感染を行い再現性の高い結果を得ることができる。

図3. タンパク質発現はMOIが高くなるほど増加する
様々な濃度のアンホトロピックレトロウイルスを含む上清で形質導入し、ZsGreen1蛍光タンパク質を発現させたNIH 3T3細胞のヒストグラム。ウイルス量の増加により感染細胞数およびZsGreen1の発現レベルが増加する。パネルA~C:MOI 0.3、3、および30での感染の結果。それぞれ8%、50%、および97%のZsGreen1陽性細胞(蛍光強度>10)が得られた(M1期細胞)。
qRT-PCR力価測定法
Retro-Xタイター測定キットには、ウイルスサンプルまたはキットに同梱のコントロールRNAを用いるqRT-PCR反応200回分の試薬が含まれている。本キットはMMLVベースのレトロウイルスベクターに使用できる。発現カセット(cDNA、shRNA)やウイルスバックボーンに左右されることなく正確な力価が得られるため、複数のウイルス試料の同時測定が可能である。RNA精製ステップおよびDNase I処理ステップがあるため、一過性トランスフェクションで産生したウイルス中にプラスミドDNAが残留していても、安定産生株から産生したウイルスと同様、少量のサンプルで正確な力価測定が行える(3)。
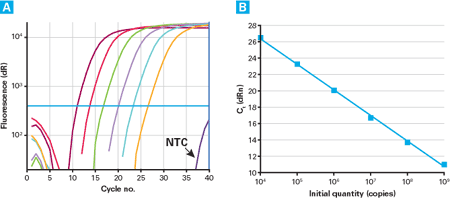
図4. Retro-X qRT-PCR力価測定法は広い測定領域をカバー
パネルA:Retro-X qRT-PCR Titration Kitを用いたリアルタイムRT-PCRで、109~104コピーのRetro-X RNA Control Templateを検出した際の増幅曲線。テンプレート無し(No-Template-Control:NTC)のバックグラウンドが低く、測定領域が6桁に及ぶことがわかる。
パネルB:パネルAの増幅曲線から得られた検量線。広い範囲のRNAコピー数に対し、高い直線性を示す。(R2:1.00、PCR効率=107.4%)
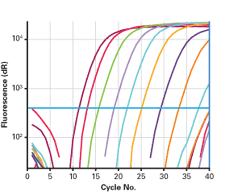
図5. Retro-X qRT-PCR Titration Kitを用いたウイルス上清の力価測定
精製した組換えレトロウイルスゲノムの10倍段階希釈液を用いたRetro-X力価測定結果の例。アンホトロピックレトロウイルスをクロンテックのRetro-X Universal Packaging Systemを用いて一過性トランスフェクションにより産生した。3日後、レトロウイルス上清を回収し、qRT-PCRによる力価測定まで-80℃で保管した。

図4. Retro-X qRT-PCR力価測定法は広い測定領域をカバー
パネルA:Retro-X qRT-PCR Titration Kitを用いたリアルタイムRT-PCRで、109~104コピーのRetro-X RNA Control Templateを検出した際の増幅曲線。テンプレート無し(No-Template-Control:NTC)のバックグラウンドが低く、測定領域が6桁に及ぶことがわかる。
パネルB:パネルAの増幅曲線から得られた検量線。広い範囲のRNAコピー数に対し、高い直線性を示す。(R2:1.00、PCR効率=107.4%)

図5. Retro-X qRT-PCR Titration Kitを用いたウイルス上清の力価測定
精製した組換えレトロウイルスゲノムの10倍段階希釈液を用いたRetro-X力価測定結果の例。アンホトロピックレトロウイルスをクロンテックのRetro-X Universal Packaging Systemを用いて一過性トランスフェクションにより産生した。3日後、レトロウイルス上清を回収し、qRT-PCRによる力価測定まで-80℃で保管した。
ウイルス感染性とRNAタイターとの相関
操作が簡便で再現性がよく、短時間で正確な結果が得られるqRT-PCR Titration Kitは、RNAタイターの測定に最適である。ウイルスストックの生物学的タイター(IFU/ml)を独立した他の方法で決定し、RNAタイター(copies/ml)との相関値(copies/IFU)をあらかじめ求めておけば、短時間で得られるRNAタイターから生物学的タイターを推定して、MOIを決定することも可能である。
表1. レトロウイルス力価測定方法の比較
表1. レトロウイルス力価測定方法の比較
| タイター相関値*1 | |||||
| パッケージング方法 | FACS(IFU/ml) | G418(cfu/ml)*2 | qRT-PCR(copies/ml) | RT:FACS (copies/IFU) |
RT:G418 (copies/cfu) |
|---|---|---|---|---|---|
| 一過性のトランスフェクション*3 | 1.1×107 | 2.9×106 | 6.3×109 | 584 | 2,176 |
| *1 | ウイルス感染力価を測定するため、ZsGreen1とG418耐性遺伝子を発現するレトロウイルスを一度qRT-PCR法で測定してから、NIH3T3細胞に感染させた。G418耐性:G418培地で細胞を12日間培養してから耐性を示すコロニーの数を染色しカウントした。FACS解析:ウイルス感染後48時間後の細胞を回収しBD FACS Caliburで解析を行った。 |
| *2 | cfu=コロニー形成単位 |
| *3 | Retro-X Universal Packaging Systemを使用した。 |
内容
Retro-X qRT-PCR Titration Kit
(製品コード 631453)
・Retro-X RNA Control Template
・Retro-X Forward and Reverse Titer Primers
・DNase I
・DNase I Buffer (10×)
・EASY Dilution Buffer for RT-PCR
・Quant-X One-Step qRT-PCR TB Green Kit (200回用)
*ウェル間の蛍光シグナルの補正を行う装置で解析する場合に使用します。
(製品コード 631453)
・Retro-X RNA Control Template
・Retro-X Forward and Reverse Titer Primers
・DNase I
・DNase I Buffer (10×)
・EASY Dilution Buffer for RT-PCR
・Quant-X One-Step qRT-PCR TB Green Kit (200回用)
・Quant-X Enzyme
・Quant-X Buffer (2×)
・RT Enzyme Mix
・RNase-Free Water
・ROX Reference Dye LSR (50×)*
・ROX Reference Dye LMP (50×)*
・NucleoSpin RNA Virus Kit (10回用)・Quant-X Buffer (2×)
・RT Enzyme Mix
・RNase-Free Water
・ROX Reference Dye LSR (50×)*
・ROX Reference Dye LMP (50×)*
*ウェル間の蛍光シグナルの補正を行う装置で解析する場合に使用します。
- ROX Reference Dye LSRを添加する機種
光源がレーザーの機種 :Applied Biosystems 7300 Real-Time PCR System (Thermo Fisher Scientific) など
(注意)StepOne/ StepOnePlus Real-Time PCR System(Thermo Fisher Scientific)はLED光源ですが、ROX Reference Dye LSRをご使用ください。 - ROX Reference Dye LMPを添加する機種
光源がLamp またはLEDの機種 :Applied Biosystems 7500/7500 Fast Real-Time PCR System(Thermo Fisher Scientific) など
保存
#631453
Retro-X RNA Control Template:-70℃
NucleoSpin RNA Virus Kit:室温
その他のコンポーネント:-20℃
Retro-X RNA Control Template:-70℃
NucleoSpin RNA Virus Kit:室温
その他のコンポーネント:-20℃
この製品を見た人は、
こんな製品も見ています
-
レンチウイルスqRT-PCR迅速タイター測定キット
-
One Step TB Green® PrimeScript™ RT-PCR Kit II (Perfect Real Time)
操作簡便な1 step RT-qPCR試薬(2コンポーネントタイプ)
-

One Step TB Green® PrimeScript™ RT-PCR Kit (Perfect Real Time)
増幅効率重視の1 step RT-qPCR試薬
-
Ecotropic Receptor Boosters
-

Retrovirus Titer Set (for Real Time PCR)
ウイルス上清から直接、4時間でRNAタイターを測定
-

Retro-X™ Concentrator
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。
