タカラバイオWEB会員募集中!
※タカラバイオWEB会員でご希望の方には、再生/細胞医療・遺伝子治療サービスにかかわる様々な情報が満載の「再生/細胞医療・遺伝子治療サービスMail News」をお届けします。
特長
- 再生医療等製品GLP適合性の認可取得をした施設で実施
- 小動物飼育・実験実施施設(AAALAC認証施設)にて実施(AAALAC:国際実験動物管理公認協会)
- 重度免疫不全動物や遺伝子組み換え生物にも対応
- 治験薬GMP/GCTP基準での再生医療等製品製造と併せたトータルサポート
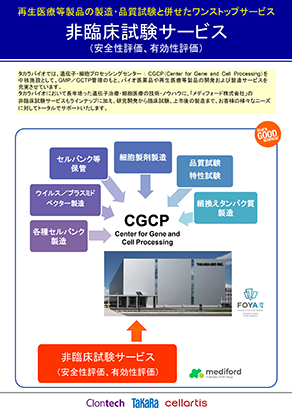
概要
タカラバイオを窓口として、非臨床試験の豊富な経験を持つ、メディフォード株式会社のGLP安全性試験をご提供いたします。
再生医療等製品それぞれに併せた単回投与毒性試験、反復投与毒性試験、in vivo造腫瘍性試験、in vitro造腫瘍性試験などをご提供します。
タカラバイオで長年培った遺伝子治療・細胞医療の技術・ノウハウを活用し、研究開発から臨床応用まで、お客様の臨床開発をトータルでサポートいたします。
タカラバイオで長年培った遺伝子治療・細胞医療の技術・ノウハウを活用し、研究開発から臨床応用まで、お客様の臨床開発をトータルでサポートいたします。
サービス内容
- 単回投与毒性試験
マウス/ラット(一般動物、病態モデル動物,免疫不全動物)を用いた各種投与経路による単回投与毒性試験の実施が可能です。投与経路は経口、経皮、皮下、静脈内、筋肉内、腹腔内、気管内など様々な経路に対応いたします。検査項目は医薬品ガイドライン反復毒性試験の検査内容(眼科検査、尿検査、血液学的検査、血液生化学的検査、剖検および病理組織学的検査)のほか、安全性薬理コアバッテリー検査、および局所刺激性検査を組み込むことも可能です。免疫染色やPCRを用いたトキシコキネティクス試験との併設も可能です。 - 反復投与毒性試験
被験細胞をマウス、ラットに反復(間歇)投与し、眼科検査、尿検査、血液学的検査、血液生化学的検査、剖検および病理組織学的検査を行います。蓄積性のある被験細胞のみが対象となります。臨床適用に合わせた試験内容をご提案いたします。 - in vitro造腫瘍性試験(軟寒天コロニー形成試験)
軟寒天コロニー形成試験法は、in vitroで行う腫瘍形成能(足場非依存性増殖能)を確認するために用いられる試験です。
デジタル軟寒天コロニー形成試験を始めとして以下3種類のin vitro造腫瘍性試験をご提供しています。試験方法 軟寒天コロニー形成試験
(従来法)軟寒天コロニー形成試験
(蛍光法)デジタル軟寒天コロニー
形成試験検出限界
または検出力hMSCに1/103(0.1%)の割合で混入する
HeLa細胞(計算上は0.02%)hMSCに1/107(0.00001%)
の割合で混入するHeLa細胞培養期間 3~4週間 約1週間 3~4週間 利点 ・ 悪性形質転換細胞を単離・特性解析できる 欠点・注意点 ・ 浮遊系細胞、iPS細胞には不適
・ 造腫瘍性細胞の有無は間接的に判断
・ 良性不死化細胞は検出不能
【関連サービス】
価格・納期
別途お問い合わせください。
納品物
別途お問い合わせください。
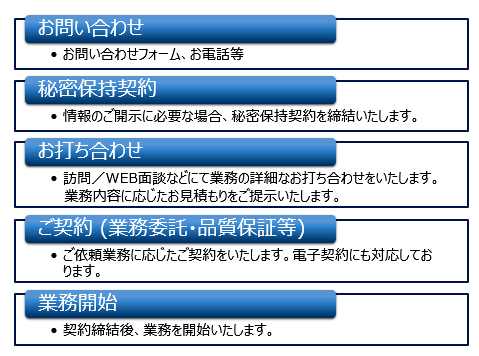
ご注文方法
受入サンプル
別途お問い合わせください。
- 注意事項
- 本受託サービスは、個別に合意した場合を除き、すべて研究目的として作業を行います。納品物を試験研究目的以外へご使用される場合、弊社では納品物に起因する損失・損害等については一切の責任を負いかねます。納品物によっては、その構成物(例えば、ベクター、蛍光色素など)の使用に制限がある場合がありますのでご注意ください。
- 納品物に起因して、直接的もしくは間接的に発生したお客様の損害については、明らかに弊社の責に帰すべき事由による場合を除いて、弊社は一切その責任を負いません。
- ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。