プロトコール A. 組換えコスミドの構築 および調製
A. 組換えコスミドの構築および調製
A-1. コスミドベクターへのインサートの挿入
組換えアデノウイルスを得るために、コスミドベクターにインサートを挿入し、組換えコスミドを作製します。コスミドベクターはいずれもクローニングサイトとしてSmi Iを持っていますので、目的遺伝子を平滑化して、Smi Iサイトにクローニングします。(pAxcwitはCla Iサイトを、またpAxCAwtit は、ClaIまたはPac Iサイトをクローニングサイトとして使用することも可能です。
- インサートDNA断片を0.5 μg程度調製する。末端が平滑でない場合、DNA Blunting Kit(製品コード 6025)等を用いて末端を平滑化する。
- インサートDNA断片を精製する。フェノール/クロロホルム抽出、エタノール沈殿を行う。
-
コスミドベクターを制限酵素Smi Iで完全に切断する。 以下の反応液を調製し、30℃で2時間インキュベーションする。
コスミドベクター 5 μl 10× H Buffer 5 μl Smi I (10 U/μl) 2 μl 滅菌精製水 up to 50 μl - 最終濃度10 mMになるようにEDTAを加えた後、フェノール/クロロホルム抽出を行う。
- A-1-2で調製したインサートDNA 0.1~0.2 μgをA-1-4に加える。
- エタノール沈殿を行う。
*コスミドを一旦乾かすと溶けなくなります。キムワイプの先で拭いて残存エタノールを除去した後、すぐ次の操作を行ってください。 - インサートDNA断片と切断したコスミドベクターとをライゲーション反応により結合させる。DNA Dissolution Buffer 5μlを加えて溶解し、Ligation Solution 5 μlを加える。25℃で10分間インキュベートする。
- エタノール沈殿を行う。
*DNAを完全に乾燥させないでください。 - 制限酵素Swa Iで切断する。
ライゲーションしたDNAに以下の試薬を加え、25℃で2時間消化する。
*この反応はインサートを持たないコスミドの出現を抑えるために重要です。ただし発現ユニット内にSmi I部位が存在する場合、この操作は行えません(A-1-13参照)。10× H Buffer 5 μl Smi I 2 μl 滅菌精製水 up to 50 μl -
適当量をλパッケージングキットでパッケージングを行う。
* 比較的大きなサイズのDNAを選択的にパッケージングするようなキット(Agilent Technologies社 Gigapack III XL Extractなど)を用いると、後の選択が容易になります。
* パッケージングキットは、ご使用されるキットの方法に従って下さい。ご参考までに下記に使用の一例を示します。
1)2×菌液を準備する。recA-の大腸菌株(DH5αなど)を前々日にプレーティングしておき、前日にシングルコロニーをピックアップしてLB培地で一晩振とう培養する。使用当日、50~100 μlを0.2%マルトース添加LB 5 mlに接種、OD650が約1.0になるまで37℃で振とう培養する(約4~6時間)。1 mlを滅菌チューブに取り、遠心し、上清を除く。ペレット(菌体)を10 mM MgSO4 500 μlに懸濁し、2×菌液とする。
2)パッケージングを行う。A-1-9.の制限酵素消化後の溶液のうち1 μlをパッケージングエクストラクトと混合して室温(22℃)で1.5時間静置する。
3)2)に、SM buffer* 100 μlを加える。
* SM buffer: NaCl 5.8 g, MgSO4・7H2O 2.0 g, 1M Tris-HCl(pH7.5) 50 ml, 2%(w/v) gelatin 5.0 ml を精製水に加え1 Lとし、オートクレーブ滅菌を行う。
4)感染を行う。3)100 μlと1)2×菌液100 μlを混合し、室温で10分静置する。
5)LB培地 1 mlを加え37℃、20分静置する。 - 大腸菌に感染させる。
- 感染させた大腸菌の1/100、1/10、残りをアンピシリンを含む寒天プレートに播く。37℃で一晩培養する。
- コスミドDNAの調製を行う。寒天培地ごとコロニーをピックアップし、アンピシリンを含むLB培地1.5 mlで培養し、コスミドDNAの調製をする。2~5 μgのコスミドDNAが調製できる。
* コスミドは大腸菌内で長く継代すると欠失しますので、大腸菌の状態でのストックは作製しないでください。
* ライゲーション後にSmi I消化した場合には、ほとんどのクローンはインサートを含んでいますので、10個程度のコロニーについて調べれば目的のクローンを得ることができます。Smi I消化を行うことができなかった場合でも、通常、24~36個のコロニーを調べれば目的のクローンが得られます。 - 制限酵素切断等により、インサートの向きと構造を確認する(A-2.構築したコスミドの構造確認)。
A-2. 構築したコスミドの構造の確認
組換えウイルスの作製には時間がかかりますので、この時点で目的どおりに組換えコスミドが構築できているか、十分に確認を行っておくことが重要です。
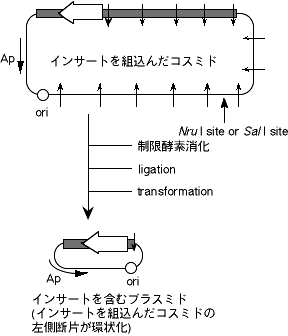
図3 アデノ落とし
コスミドのサイズは40 kbpを超えるため、インサートの構造や方向を確認するのが困難な場合がある。
そのような場合には、コスミドをNru IまたはSal I(インサート内にサイトがない制限酵素)で消化して、ライゲーションし、大腸菌にトランスフォーメーションすることにより、インサートを含むプラスミドが得られる。
得られたプラスミドはインサート、大腸菌で働く複製起点およびアンピシリン耐性遺伝子を含んでいるが、アデノウイルスゲノムのほとんどを欠失しているため、サイズが小さく扱いやすい。このプラスミドを用いて構造や方向を確認する。また、高発現プラスミドとして有用である。
- インサートの入っているコスミドクローンを選択する。Cla Iで消化することによりインサートを切り出すことができる。
-
インサートの向きの確認を行う。インサートの方向は、適当な制限酵素で切断することにより確認できる。(「IV-2. コスミドベクターの構造」)
* Nru IまたはSal Iで切断し、ライゲーションすることにより、アデノウイルスゲノムのほとんどを欠失したプラスミドを得ることができます(「アデノ落とし」、図3)。構築確認のための適当な制限酵素サイトがない場合、得られたプラスミド(「アデノ落としプラスミド」)をもちいて構造を確認することもできます。 - この時点で適当なtransfection法により細胞に「アデノ落としプラスミド」またはコスミドDNAを導入し、目的遺伝子の発現を確認しておく。
*「アデノ落としプラスミド」は発現プラスミドとして有用です。

コスミドのサイズは40 kbpを超えるため、インサートの構造や方向を確認するのが困難な場合がある。
そのような場合には、コスミドをNru IまたはSal I(インサート内にサイトがない制限酵素)で消化して、ライゲーションし、大腸菌にトランスフォーメーションすることにより、インサートを含むプラスミドが得られる。
得られたプラスミドはインサート、大腸菌で働く複製起点およびアンピシリン耐性遺伝子を含んでいるが、アデノウイルスゲノムのほとんどを欠失しているため、サイズが小さく扱いやすい。このプラスミドを用いて構造や方向を確認する。また、高発現プラスミドとして有用である。
A-3. 構築したコスミドの大量調製
コスミドは大腸菌内で長く継代すると欠失するので、以下に示す方法で増やしてDNAの状態で保存し、293細胞へのtransfectionに利用する。
- コスミド(環状のまま)をλパッケージングキットでパッケージングし大腸菌に感染させる。
- アンピシリンを含むLB培地で培養する。1/100量をプレートに播き、残りを 液体培地50 mlに加える。
- プレートのコロニーが10個以上なら、50 mlの液体培地からコスミドDNAを調製する。プレートのコロニーが10個以下なら、液体培地の大腸菌が増殖していても(長く継代しすぎていることになるので)廃棄してやり直す。
- コスミドDNAをtransfectionを行うのに十分な程度精製する。CsCl濃度勾配遠心法や適当なDNA調製用キットを用いる。
