コンピテントセルHST16CR株を使用した実験例
遺伝子pcnB(plasmid copy number B)を欠損した株であるHST16CRは、pUC系ベクターのコピー数を低く維持する性質を持ちます。
そのため、高コピーベクターではクローニングの難しい膜貫通ドメインを持つタンパクや細胞毒性を持つタンパクなど、大腸菌の生育を阻害する遺伝子のクローニングを可能にすることが期待されます。
そのため、高コピーベクターではクローニングの難しい膜貫通ドメインを持つタンパクや細胞毒性を持つタンパクなど、大腸菌の生育を阻害する遺伝子のクローニングを可能にすることが期待されます。
【実験例1:本製品とHST08株とのコピー数の比較】
|
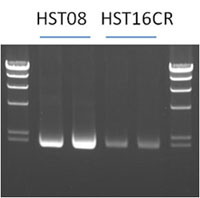
プラスミドpUC19で形質転換したpcnB欠損株「HST16CR」及び非欠損株「HST08
Premium」培養し、プラスミド精製後、抽出プラスミド量を比較しました。 <方法> 各株を一晩液体培養し、OD600の値が同じになるよう調製した後、同じ条件でプラスミドDNA精製キットを使用し精製を行った。 溶出は50 μl TEで行い、溶出液量各1 μLを泳動ゲル各レーンにアプライした。 <結果> pcnB欠損株「HST16CR」は、非欠損株「HST08 Premium」に比べ、抽出プラスミド量が少ないことが確認できました。 |
|
【実験例2 :大腸菌の生育を阻害する遺伝子のクローニング①遺伝子mazFのクローニング】
MazFは、大腸菌のトキシン-アンチトキシンモジュールのトキシンタンパク質で、一本鎖RNA中のACA配列を認識し特異的に切断するエンド型リボヌクレアーゼ活性を有しています。
MazF遺伝子をベクターに挿入し、PcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用して形質転換の効率を比較しました。
<方法>
大腸菌のMazF遺伝子をpUC118 vector(ΔlacO)にIn Frameでクローニングした。
取得した単一plasmid DNAを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08Premium」「DH5α」では強い生育阻害がかかり、コロニーが得られませんでした。
一方、PcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC-mazF plasmid

MazF遺伝子をベクターに挿入し、PcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用して形質転換の効率を比較しました。
<方法>
大腸菌のMazF遺伝子をpUC118 vector(ΔlacO)にIn Frameでクローニングした。
取得した単一plasmid DNAを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08Premium」「DH5α」では強い生育阻害がかかり、コロニーが得られませんでした。
一方、PcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC-mazF plasmid

【実験例3:大腸菌の生育を阻害する遺伝子のクローニング②膜タンパク質遺伝子dpiBのクローニング】
遺伝子dpiBは、大腸菌の膜タンパク質DpiABのコンポーネントであるmembrane associated sensor kinaseをコードします。
dpiBをベクターに挿入し、pcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用して形質転換の効率を比較しました。
<方法>
dpi遺伝子をPCRで増幅し、pUC118 vectorにLigationした。このLigation Mixを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08 Premium」「DH5α」では強い生育阻害がかかり、コロニーがほとんど得られませんでした。一方、pcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC-dpiB Ligation Mix

dpiBをベクターに挿入し、pcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用して形質転換の効率を比較しました。
<方法>
dpi遺伝子をPCRで増幅し、pUC118 vectorにLigationした。このLigation Mixを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08 Premium」「DH5α」では強い生育阻害がかかり、コロニーがほとんど得られませんでした。一方、pcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC-dpiB Ligation Mix

【実験例4:大腸菌の生育を阻害する遺伝子のクローニング③膜タンパク質遺伝子IspAのクローニング】
遺伝子lspAは、大腸菌の4回膜貫通タンパク質prolipoprotein signal peptidase (signal peptidase II)をコードします。
lspAをベクターに挿入し、pcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用し形質転換の効率を比較しました。
<方法>
lspA遺伝子をPCRで増幅し、pUC118 vectorにLigationした。このLigation Mixを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08premium」「DH5α」では強い生育阻害がかかり、コロニーがほとんど得られませんでした。一方、pcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC118_lspA Lgation Mix

lspAをベクターに挿入し、pcnB欠損株「HST16CR」及び非欠損株「HST08 Premium」「DH5α」を使用し形質転換の効率を比較しました。
<方法>
lspA遺伝子をPCRで増幅し、pUC118 vectorにLigationした。このLigation Mixを、各コンピテントセルに導入した。
LB/Amp/IPTG/X-gal寒天培地にplating後、37度、15時間培養した。
<結果>
「HST08premium」「DH5α」では強い生育阻害がかかり、コロニーがほとんど得られませんでした。一方、pcnB欠損株「HST16CR」では多くのコロニーが得られました。
DNA:pUC118_lspA Lgation Mix

