Human Cell-Free Protein Expression Master Mix for mRNA(製品コード 3288)を用いたタンパク質の無細胞発現
Takara IVTpro T7 mRNA Synthesis Kit(製品コード 6144)を用いて作製したmRNAを使用して、Human Cell-Free Protein Expression Master Mix for mRNA(製品コード 3288)によりタンパク質の無細胞発現を行った。
1.分子量の異なる3種類のタンパク質の無細胞発現 ーRNA添加量、反応時間、反応温度による影響の評価ー
Cloning Kit for mRNA Template (BspQ I)(製品コード 6133)、Takara IVTpro T7 mRNA Synthesis Kit(製品コード 6144)、およびCleanCap Reagent AG (3’OMe) (TriLink社) を用いて、3種類(eIF4G、FLuc、ZsGreen)のキャップ化mRNAおよび非キャップ化RNAを合成した。
■反応時間の影響
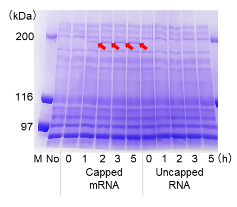
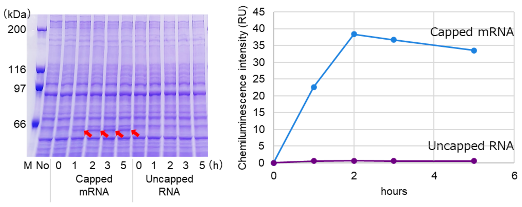
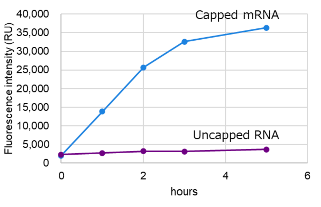 図1-A. 反応時間の評価
図1-A. 反応時間の評価
3種類のキャップ化mRNAおよび非キャップ化RNAそれぞれ2 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、32℃で0、1、2、3および5時間インキュベートした。
その結果、キャップ化mRNAの添加においてのみ目的タンパク質の高い発現が確認された。
これにより、本無細胞発現系においてはmRNAの発現がキャップ依存的であることが示された。
また、eIF4Gでは3~5時間、FLucでは2時間、ZsGreenでは5時間でタンパク質の発現が最大化されたことから、タンパク質によって最適な反応時間が異なることが示された。
■mRNA添加量の影響

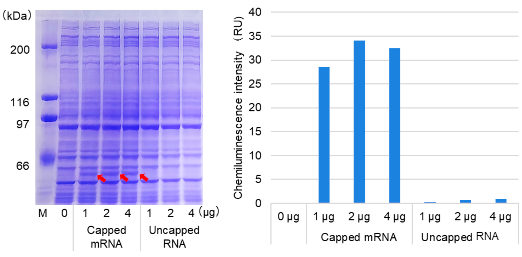
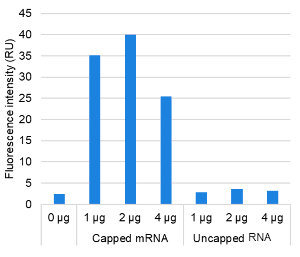 図1-B. mRNA添加量の評価
図1-B. mRNA添加量の評価
3種類のキャップ化mRNAおよび非キャップ化RNAそれぞれ1、2、4 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、32℃で3時間インキュベートした。
その結果、いずれのタンパク質も2 μgのmRNA添加によって発現が最大化されることが示された。※
※:キャップ化mRNA量は2 μgを推奨しますが、目的タンパク質の産生が少ない場合は、添加量を変更してお試しください。
■反応温度の影響
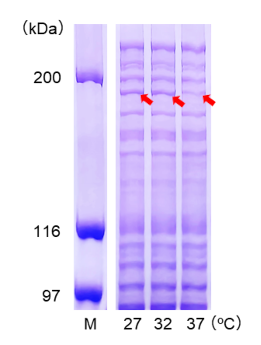
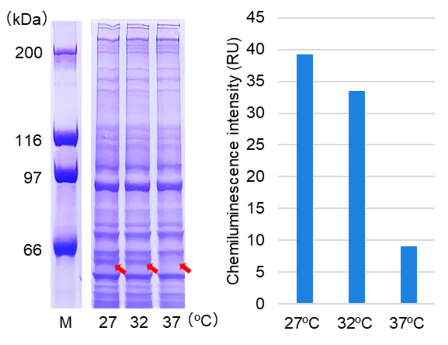
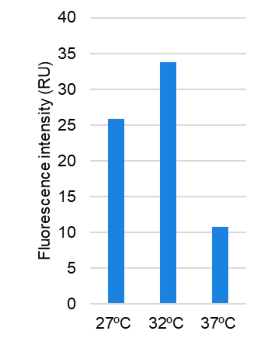 図1-C. 反応温度の評価
図1-C. 反応温度の評価
3種類のキャップ化mRNAそれぞれ2 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、27℃、32℃および37℃で3時間インキュベートした。
その結果、eIF4Gは27℃または32℃、FLucでは27℃、ZsGreenでは32℃でタンパク質の発現が最大化された。
これにより、本無細胞発現系においては、タンパク質によって最適な反応温度が異なることが示された。
2. RNA配列(3’ UTRの種類)が翻訳効率に与える影響と細胞発現との相関
キャップ化FLuc mRNAを使用し、Human Cell-Free Protein Expression Master Mix for mRNA(製品コード 3288)を用いた無細胞発現と、HEK293T細胞およびHeLa S3細胞を用いた細胞発現の相関を評価した。
■本実験で使用したキャップ化FLuc mRNAの調製手順

図2-A. 本実験で使用した鋳型DNA
■無細胞発現と細胞発現の相関
Master Mix for mRNA
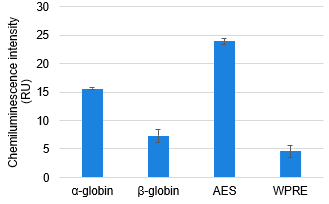
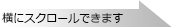
図2-B. 無細胞発現と細胞発現の相関
無細胞発現系として、各キャップ化FLuc mRNAを2 μgずつHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、27℃で2時間インキュベートした。
一方、細胞発現系として、同mRNAをHEK293T細胞およびHeLa S3細胞にTransIT-mRNA Transfection Reagent(製品コード MIR2225)を用いて0.5 μgトランスフェクションし、24時間培養した。
これらの反応後、サンプルの一部を用いてFLucタンパク質の活性を化学発光測定した。
その結果、無細胞発現系と細胞発現系の比較において、FLucタンパク質の発現レベルに相関が確認された。
これにより、mRNAを使用した無細胞発現系が、mRNA構築物の評価やスクリーニングにとって簡便かつ迅速な手段となり得ることが示された。
1.分子量の異なる3種類のタンパク質の無細胞発現 ーRNA添加量、反応時間、反応温度による影響の評価ー
Cloning Kit for mRNA Template (BspQ I)(製品コード 6133)、Takara IVTpro T7 mRNA Synthesis Kit(製品コード 6144)、およびCleanCap Reagent AG (3’OMe) (TriLink社) を用いて、3種類(eIF4G、FLuc、ZsGreen)のキャップ化mRNAおよび非キャップ化RNAを合成した。
■反応時間の影響
eIF4G

FLuc

ZsGreen

3種類のキャップ化mRNAおよび非キャップ化RNAそれぞれ2 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、32℃で0、1、2、3および5時間インキュベートした。
その結果、キャップ化mRNAの添加においてのみ目的タンパク質の高い発現が確認された。
これにより、本無細胞発現系においてはmRNAの発現がキャップ依存的であることが示された。
また、eIF4Gでは3~5時間、FLucでは2時間、ZsGreenでは5時間でタンパク質の発現が最大化されたことから、タンパク質によって最適な反応時間が異なることが示された。
■mRNA添加量の影響
eIF4G

FLuc

ZsGreen

3種類のキャップ化mRNAおよび非キャップ化RNAそれぞれ1、2、4 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、32℃で3時間インキュベートした。
その結果、いずれのタンパク質も2 μgのmRNA添加によって発現が最大化されることが示された。※
※:キャップ化mRNA量は2 μgを推奨しますが、目的タンパク質の産生が少ない場合は、添加量を変更してお試しください。
■反応温度の影響
eIF4G

FLuc

ZsGreen

3種類のキャップ化mRNAそれぞれ2 μgずつをHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、27℃、32℃および37℃で3時間インキュベートした。
その結果、eIF4Gは27℃または32℃、FLucでは27℃、ZsGreenでは32℃でタンパク質の発現が最大化された。
これにより、本無細胞発現系においては、タンパク質によって最適な反応温度が異なることが示された。
2. RNA配列(3’ UTRの種類)が翻訳効率に与える影響と細胞発現との相関
キャップ化FLuc mRNAを使用し、Human Cell-Free Protein Expression Master Mix for mRNA(製品コード 3288)を用いた無細胞発現と、HEK293T細胞およびHeLa S3細胞を用いた細胞発現の相関を評価した。
■本実験で使用したキャップ化FLuc mRNAの調製手順
- ヒトのα-globin、β-globin、AES遺伝子由来の3’-UTR配列、および肝炎ウイルス由来のWPRE配列のいずれかをFLuc遺伝子の下流(図2-A:オレンジ部分)に挿入した鋳型DNAを用意
- Takara IVTpro T7 mRNA Synthesis Kit(製品コード 6144)およびCleanCap AG (3’ OMe)(TriLink社)を使用してキャップ化mRNAを合成

図2-A. 本実験で使用した鋳型DNA
表. 挿入配列
| 1. | ヒトα-globin由来の3’-UTR |
| 2. | ヒトβ-globin由来の3’-UTR |
| 3. | ヒトAES遺伝子由来の3’-UTR |
| 4. | 肝炎ウイルス由来のWPRE |
■無細胞発現と細胞発現の相関
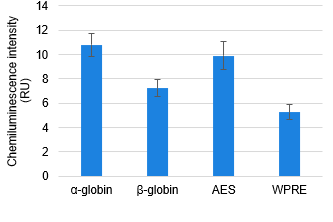
無細胞発現
Human Cell-Free Protein ExpressionMaster Mix for mRNA

細胞発現
HEK293T細胞
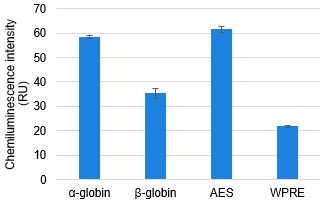

相関(HEK293T細胞)
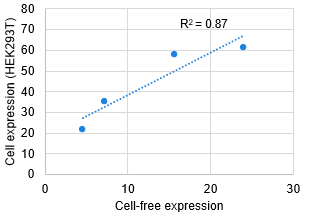

HeLa S3細胞

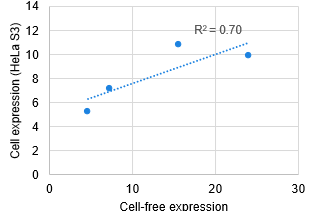
相関(HeLa S3細胞)

無細胞発現系として、各キャップ化FLuc mRNAを2 μgずつHuman Cell-Free Protein Expression Master Mix for mRNAに添加し、27℃で2時間インキュベートした。
一方、細胞発現系として、同mRNAをHEK293T細胞およびHeLa S3細胞にTransIT-mRNA Transfection Reagent(製品コード MIR2225)を用いて0.5 μgトランスフェクションし、24時間培養した。
これらの反応後、サンプルの一部を用いてFLucタンパク質の活性を化学発光測定した。
その結果、無細胞発現系と細胞発現系の比較において、FLucタンパク質の発現レベルに相関が確認された。
これにより、mRNAを使用した無細胞発現系が、mRNA構築物の評価やスクリーニングにとって簡便かつ迅速な手段となり得ることが示された。
