AAVベクター作製における産生細胞由来ゲノムDNAの除去効果
【目的】
AAVベクター製造では、AAVの凝集を防ぐため高塩濃度条件下で細胞を溶解する。
そのため、その後の核酸分解工程では、高塩濃度のサンプルから核酸を除去することが求められる。
低温・高塩濃度条件で活性を維持する本製品を用いることで、高塩濃度のサンプルから産生細胞由来のゲノムDNAを効率的に除去することを目的とした。
【方法】
AAVpro Helper Free System (AAV2)(製品コード 6230)を使用してHEK293細胞にてAAVを産生させ、回収した細胞及び培養上清からAAVを抽出した(塩濃度条件:500 mM)。産生細胞由来のゲノムDNAを除去するため、本製品、他社酵素、NucleoGone Endonuclease(製品コード 2490A)を10、25、50 U/mlになるように添加し、37℃で1時間処理した。処理後のサンプルを遠心し、上清をフィルターろ過したものをAAV抽出液として以下の実験を行った。データは独立した3回の平均値を示す。(弊社取得データ)
 (A)AAVベクター中に残留した産生細胞由来のゲノムDNA
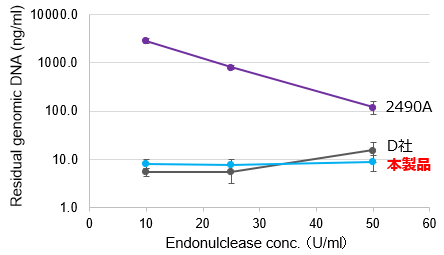
(A)AAVベクター中に残留した産生細胞由来のゲノムDNA
AAV抽出液に残留した細胞由来ゲノムDNAを、dPCRにより測定した。
その結果、本製品は10 U/mlでの使用においても残留ゲノム濃度が低く、産生細胞由来ゲノムDNAを除去する効果が高いことが示された。
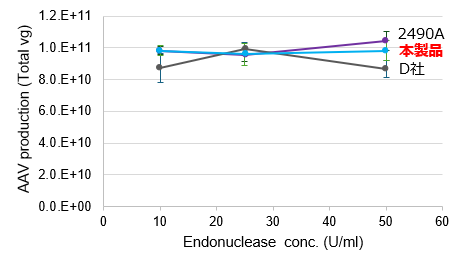
(B)AAVベクター力価への影響
取得したAAVベクターの力価を、AAVpro Titration Kit (for Real Time PCR) Ver.2(製品コード 6233)を用いたqPCR法により測定した。
その結果、本製品を用いた核酸除去処理は、AAVベクターの力価に影響を与えないことが示された。
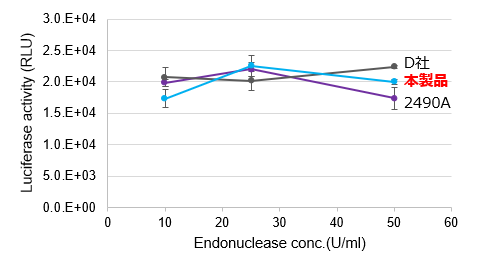
(C)遺伝子導入効率の評価
293T細胞にAAV抽出液を感染し(多重感染度(MOI=100))、3日後、導入遺伝子であるルシフェラーゼの活性を測定した。
その結果、本製品を用いた核酸除去処理は、 AAVベクターの感染性には影響を与えないことが示された。
AAVベクター製造では、AAVの凝集を防ぐため高塩濃度条件下で細胞を溶解する。
そのため、その後の核酸分解工程では、高塩濃度のサンプルから核酸を除去することが求められる。
低温・高塩濃度条件で活性を維持する本製品を用いることで、高塩濃度のサンプルから産生細胞由来のゲノムDNAを効率的に除去することを目的とした。
【方法】
AAVpro Helper Free System (AAV2)(製品コード 6230)を使用してHEK293細胞にてAAVを産生させ、回収した細胞及び培養上清からAAVを抽出した(塩濃度条件:500 mM)。産生細胞由来のゲノムDNAを除去するため、本製品、他社酵素、NucleoGone Endonuclease(製品コード 2490A)を10、25、50 U/mlになるように添加し、37℃で1時間処理した。処理後のサンプルを遠心し、上清をフィルターろ過したものをAAV抽出液として以下の実験を行った。データは独立した3回の平均値を示す。(弊社取得データ)
A
AAV抽出液に残留した産生細胞由来のゲノムDNA
B
AAVベクター力価への影響
C
遺伝子導入効率の評価
AAV抽出液に残留した細胞由来ゲノムDNAを、dPCRにより測定した。
その結果、本製品は10 U/mlでの使用においても残留ゲノム濃度が低く、産生細胞由来ゲノムDNAを除去する効果が高いことが示された。
(B)AAVベクター力価への影響
取得したAAVベクターの力価を、AAVpro Titration Kit (for Real Time PCR) Ver.2(製品コード 6233)を用いたqPCR法により測定した。
その結果、本製品を用いた核酸除去処理は、AAVベクターの力価に影響を与えないことが示された。
(C)遺伝子導入効率の評価
293T細胞にAAV抽出液を感染し(多重感染度(MOI=100))、3日後、導入遺伝子であるルシフェラーゼの活性を測定した。
その結果、本製品を用いた核酸除去処理は、 AAVベクターの感染性には影響を与えないことが示された。
