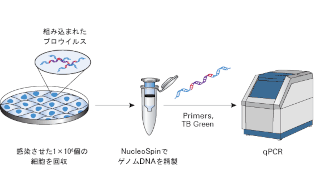
レンチウイルスによるT細胞への遺伝子導入を迅速かつ効率的に
- 24ウェルサイズの多孔性スポンジを用い、T細胞の活性化とレンチウイルスによる遺伝子導入を1ステップで実施
- スポンジ内にT細胞活性化因子が含まれており、レンチウイルス導入前のT細胞活性化は不要
- 遠心感染やポリブレンなどの導入促進剤は不要。細胞へのダメージを低減
- 1つのスポンジで2×106~1×107個のT細胞、PBMCが使用可能
- マイクロ流体ベースの特別な機器を用いることなく、同様の効果を実現
無料サンプルご提供中!
サンプルのお申し込みはこちらから
サンプルのお申し込みはこちらから
製品説明
Lenti-X T-Cell Transduction Spongeは、多孔性のアルギン酸塩で構成されたスポンジ状の製品で、T細胞やPBMCに対して簡便かつ効率的にレンチウイルスを導入することができます。スポンジには、T細胞活性化試薬(rhIL-2(100 IU)、抗ヒトCD3抗体、抗ヒトCD28抗体)が最適な比率で含まれているため、事前にT細胞を活性化する必要はなく、細胞の活性化とウイルス導入を1ステップで行うことが可能です。
スポンジの微細な流路構造の中で、活性化されたT細胞とレンチウイルスが局在することにより、時間を要する遠心感染法や細胞への影響が懸念される化学的な導入促進剤を用いることなく、迅速、かつ効率的に細胞への遺伝子導入が促進されます。導入後は、専用のRelease Bufferを加えることで細胞をスポンジから容易に回収できます。24ウェルプレートサイズのため少ない液量で使用でき、1つのスポンジで2×106~1×107個のT細胞またはPBMCに対応します。特別な機器は不要で、簡便な操作手順により、細胞操作を最小限に抑えつつ、従来法と同等またはそれ以上の導入効率が得られます。
スポンジの微細な流路構造の中で、活性化されたT細胞とレンチウイルスが局在することにより、時間を要する遠心感染法や細胞への影響が懸念される化学的な導入促進剤を用いることなく、迅速、かつ効率的に細胞への遺伝子導入が促進されます。導入後は、専用のRelease Bufferを加えることで細胞をスポンジから容易に回収できます。24ウェルプレートサイズのため少ない液量で使用でき、1つのスポンジで2×106~1×107個のT細胞またはPBMCに対応します。特別な機器は不要で、簡便な操作手順により、細胞操作を最小限に抑えつつ、従来法と同等またはそれ以上の導入効率が得られます。
簡便な使用方法
T細胞またはPBMCとレンチウイルスを混合してスポンジに添加し、37℃で1時間インキュベートしてスポンジに混合液を吸収させます。次に、培地を加えて37℃で48時間インキュベートします。インキュベーション後、特殊なRelease Bufferを加えてスポンジを溶解し、細胞を回収します。
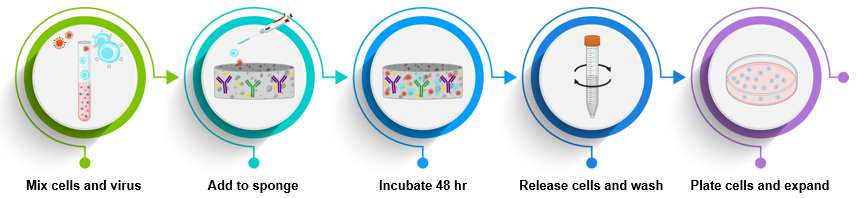
図1.Lenti-X T-Cell Transduction Spongeのワークフロー
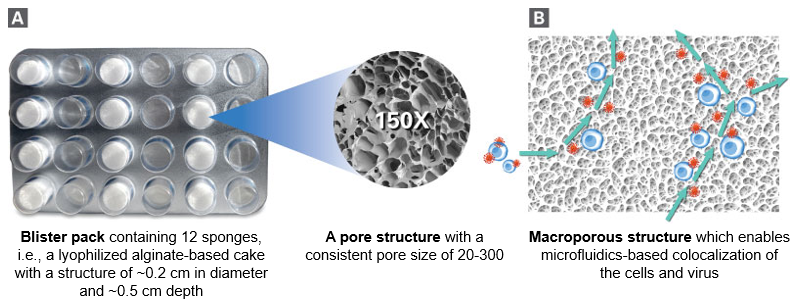
図2.Lenti-X T-Cell Transduction Spongeの詳細
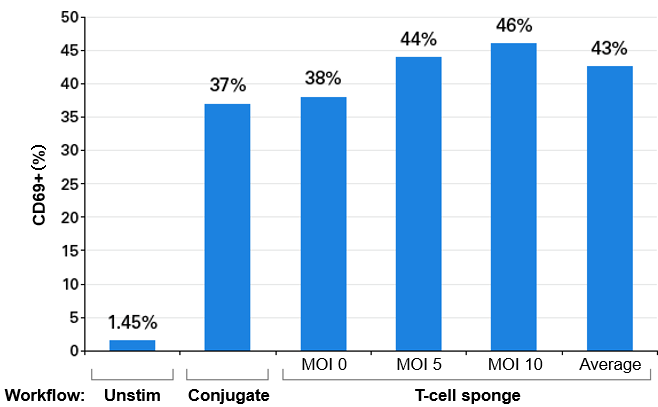
図3.T細胞活性化
Lenti-X T-Cell Transduction SpongeまたはT細胞活性化試薬を用いて、T細胞の活性化効果を比較した。4×106個のヒト初代T細胞を用いて、ZsGreen1発現レンチウイルスをMOI=5、10で混合してLenti-X T-Cell Transduction Spongeで処理(T-cell sponge)、あるいはImmunoCult Human CD3/CD28 T Cell Activator(STEMCELL Technologies社)で刺激した(Conjugate)。また、コントロールとして未刺激の細胞を用いた(Unstim)。それぞれ48時間後にFCM解析によりCD69+の発現率を測定してT細胞の活性化レベルを調べた。
その結果、本製品で処理した細胞は、T細胞活性化試薬で処理した細胞と同等以上の発現率を示した。よって、本製品はT細胞を十分に活性化できることが示された。
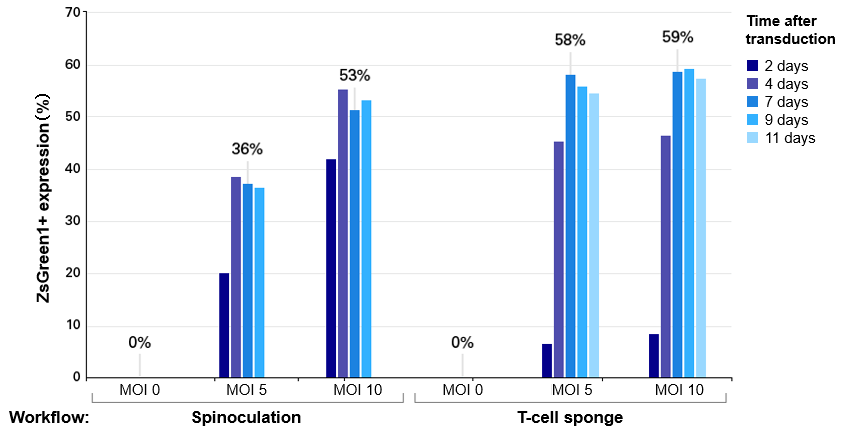
図4.ヒト初代T細胞への遺伝子導入効率
4×106個のヒト初代T細胞に、遠心感染法またはLenti-X T-Cell Transduction Spongeを使用して、MOI=5、10でZsGreen1発現レンチウイルスによる遺伝子導入(トランスダクション)を実施した。遠心感染法は、ImmunoCult Human CD3/CD28 T Cell Activator(STEMCELL Technologies社)で2日間 T細胞を活性化した後にレンチウイルスを添加し、ポリブレン(8 μg/ml)存在下で、1,500×gで90分間遠心した(Spinoculation)。遺伝子導入後、FCM解析によりZsGreen1の発現を経時的に測定し、遺伝子導入効率を評価した。グラフ中に表示されている数値(%)は、7日目におけるZsGreen1陽性(ZsGreen1+)率を示している。
その結果、本製品を用いた場合、遠心感染法と同等以上の導入効率が得られることが示された。
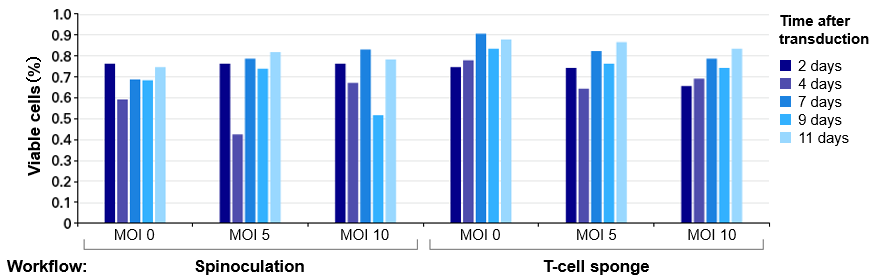
図5.ヒト初代T細胞への遺伝子導入後の細胞生存率
4×106個のヒト初代T細胞に、遠心感染法またはLenti-X T-Cell Transduction Spongeを使用して、MOI=5、10で ZsGreen1発現レンチウイルスによる遺伝子導入(トランスダクション)を実施した。遠心感染法は、CD3/CD28 ImmunoCult試薬でT細胞を2日間活性化した後にレンチウイルスを添加し、ポリブレン(8 μg/ml)存在下で、1,500×gで90分間遠心した(Spinoculation)。遺伝子導入後、細胞の生存率を7-AAD染色およびFCM解析により経時的に測定した。
その結果、本製品を用いた遺伝子導入後の細胞生存率は、遠心感染法よりも高く維持されることが示された。

図1.Lenti-X T-Cell Transduction Spongeのワークフロー
- ターゲット細胞とレンチウイルスを混合する(トータル液量の上限は150 μl)
- スポンジを24ウェルプレートにセットし、細胞とウイルスの混合液を滴下する
- 37℃で1時間インキュベート後、培地を添加して48時間インキュベートする
- インキュベート後、培地とスポンジを15 mlチューブに移し、Release Bufferを添加、遠心してスポンジを溶解し、PBSで2回Washする
- 細胞を新しい培養容器に移して培養を開始する

図2.Lenti-X T-Cell Transduction Spongeの詳細
Panel A:製品外観とスポンジ構造の拡大図。12個のスポンジが個別にパックされている。
スポンジサイズ:直径~0.2 cm、高さ~0.5 cm
ポアサイズ:20~300 μm
スポンジサイズ:直径~0.2 cm、高さ~0.5 cm
ポアサイズ:20~300 μm
Panel B:微細な流路構造内で細胞とウイルスが局在する様子(イメージ図)

図3.T細胞活性化
Lenti-X T-Cell Transduction SpongeまたはT細胞活性化試薬を用いて、T細胞の活性化効果を比較した。4×106個のヒト初代T細胞を用いて、ZsGreen1発現レンチウイルスをMOI=5、10で混合してLenti-X T-Cell Transduction Spongeで処理(T-cell sponge)、あるいはImmunoCult Human CD3/CD28 T Cell Activator(STEMCELL Technologies社)で刺激した(Conjugate)。また、コントロールとして未刺激の細胞を用いた(Unstim)。それぞれ48時間後にFCM解析によりCD69+の発現率を測定してT細胞の活性化レベルを調べた。
その結果、本製品で処理した細胞は、T細胞活性化試薬で処理した細胞と同等以上の発現率を示した。よって、本製品はT細胞を十分に活性化できることが示された。

図4.ヒト初代T細胞への遺伝子導入効率
4×106個のヒト初代T細胞に、遠心感染法またはLenti-X T-Cell Transduction Spongeを使用して、MOI=5、10でZsGreen1発現レンチウイルスによる遺伝子導入(トランスダクション)を実施した。遠心感染法は、ImmunoCult Human CD3/CD28 T Cell Activator(STEMCELL Technologies社)で2日間 T細胞を活性化した後にレンチウイルスを添加し、ポリブレン(8 μg/ml)存在下で、1,500×gで90分間遠心した(Spinoculation)。遺伝子導入後、FCM解析によりZsGreen1の発現を経時的に測定し、遺伝子導入効率を評価した。グラフ中に表示されている数値(%)は、7日目におけるZsGreen1陽性(ZsGreen1+)率を示している。
その結果、本製品を用いた場合、遠心感染法と同等以上の導入効率が得られることが示された。

図5.ヒト初代T細胞への遺伝子導入後の細胞生存率
4×106個のヒト初代T細胞に、遠心感染法またはLenti-X T-Cell Transduction Spongeを使用して、MOI=5、10で ZsGreen1発現レンチウイルスによる遺伝子導入(トランスダクション)を実施した。遠心感染法は、CD3/CD28 ImmunoCult試薬でT細胞を2日間活性化した後にレンチウイルスを添加し、ポリブレン(8 μg/ml)存在下で、1,500×gで90分間遠心した(Spinoculation)。遺伝子導入後、細胞の生存率を7-AAD染色およびFCM解析により経時的に測定した。
その結果、本製品を用いた遺伝子導入後の細胞生存率は、遠心感染法よりも高く維持されることが示された。
内容
- Lenti-X T-Cell Transduction Sponge 12個
- Release Buffer 30 ml
- ピンセット 1個
保存
4℃
(Lenti-X T-Cell Transduction Spongeは乾燥剤入りのパウチに入れたまま保存)
(Lenti-X T-Cell Transduction Spongeは乾燥剤入りのパウチに入れたまま保存)
本製品以外に必要な試薬、機器(主なもの)
- 1×PBS containing Ca2+ and Mg2+
- T細胞用完全培地(例:LymphoONE T-Cell Expansion Xeno-Free Medium(製品コード WK552SまたはWK552))
- 24ウェルプレート(ノントリートメントタイプ)*必ず未処理のプレートをご使用ください。
- 15 mlチューブ
- 遠心機(15 mlチューブ対応)
- インキュベーター
ImmunoCultはSTEMCELL Technologies社のトレードマークです。
関連製品・受託
LymphoONE® T-Cell Expansion Xeno-Free Medium
Lenti-X™ Transduction Sponge
Lenti-X™ 293T細胞株
pLVSIN-CMV/EF1α Vector
pLVSIN蛍光タンパク質ベクター
Lentiviral High Titer Packaging Mix with pLVSINシリーズ
LVpro™ Packaging Mix with pLVproシリーズ
LVpro™ Packaging Mix with pLVpro Purシリーズ
Lenti-X™ インテグラーゼ欠損レンチウイルスパッケージング試薬
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。