製品説明
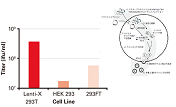
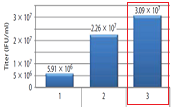
pLVSIN Vectorは、SIN型(自己不活性型)のレンチウイルスベクタープラスミドである。本製品と新しく開発したLentiviral High Titer Packaging Mix(製品コード 6194)を組み合わせて用いることで、パントロピックなVSV-Gシュードタイプの組換えレンチウイルスを高力価で調製することができ、初代培養細胞、非分裂細胞を含むほぼすべての哺乳類細胞に遺伝子導入が可能となる。(図1)
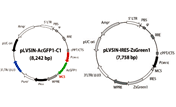
pLVSIN-CMV Vectorではマルチクローニングサイトに挿入した目的遺伝子がCMVプロモーターにより発現する。PGKプロモーターの下流には薬剤耐性遺伝子(ネオマイシン耐性、ハイグロマイシン耐性、またはピューロマイシン耐性)が搭載されており、安定発現株の選択に利用できる。
また、mRNAを安定化するWPRE(woodchuck hepatitis virus post-transcriptional regulatory element)配列、ウイルスゲノムの核移行や宿主染色体への組換え効率を高めるcPPT(central polypurine tract)配列なども含まれ、高力価レンチウイルスの産生および導入遺伝子の高発現に寄与している。
pLVSIN-EF1α Vectorは、CMVプロモーターに替えて、ヒトポリペプチド鎖伸長因子遺伝子プロモーター(EF1αプロモーター)を搭載しており、CMVプロモーターで発現レベルが低い場合や、胚性幹細胞のようにプロモーターがサイレンシングを受ける場合に有用である(図2)。
ZsGreen1遺伝子を挿入したpLVSIN-CMV Pur VectorとLentiviral High Titer Packaging Mixを組み合わせて取得したZsGreen1発現レンチウイルスベクター上清を、各標的細胞への感染に使用した。感染にはRetroNectinを使用し、RBV-Spin法で行った。
この組み合わせで得たレンチウイルス上清は、多くの場合、濃縮しないで直接、標的細胞への感染に使用できる。
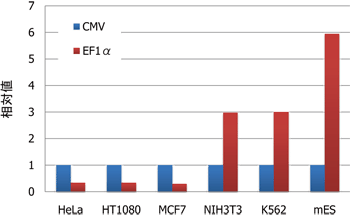
図2. EF1αプロモーターとCMVプロモーターの発現強度の比較(1 copy/cellでの相対値)
ZsGreen1遺伝子を挿入したpLVSIN-CMV PurまたはpLVSIN-EF1α Purベクターと、クロンテックLenti-X HTX Packaging System、Lenti-X 293T細胞を用いて組換えレンチウイルスを調製した。ウイルス上清の段階希釈液を用い、ポリブレン法、あるいはRetroNectin法で各細胞への感染を行い、2~3日後にフローサイトメーターを用いて遺伝子導入効率ならびにZsGreen1発現強度を測定した。遺伝子導入効率が20%以下のサンプルをsingle copy導入細胞とみなし、CMVプロモーターとEF1αプロモーターの発現強度を比較した。グラフではCMVプロモーターの発現強度を1とした場合の相対値を示している。
pLVSIN-CMV Vectorではマルチクローニングサイトに挿入した目的遺伝子がCMVプロモーターにより発現する。PGKプロモーターの下流には薬剤耐性遺伝子(ネオマイシン耐性、ハイグロマイシン耐性、またはピューロマイシン耐性)が搭載されており、安定発現株の選択に利用できる。
また、mRNAを安定化するWPRE(woodchuck hepatitis virus post-transcriptional regulatory element)配列、ウイルスゲノムの核移行や宿主染色体への組換え効率を高めるcPPT(central polypurine tract)配列なども含まれ、高力価レンチウイルスの産生および導入遺伝子の高発現に寄与している。
pLVSIN-EF1α Vectorは、CMVプロモーターに替えて、ヒトポリペプチド鎖伸長因子遺伝子プロモーター(EF1αプロモーター)を搭載しており、CMVプロモーターで発現レベルが低い場合や、胚性幹細胞のようにプロモーターがサイレンシングを受ける場合に有用である(図2)。
-
-
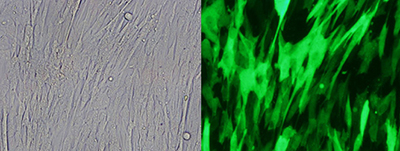
A)初代ヒト腸筋線維芽細胞への感染
・90 倍希釈したレンチウイルス(MOI=12.4)を感染
・感染5日後:ZsGreen1 陽性率69.2% -
-
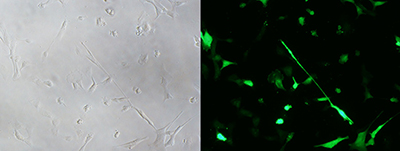
B)ヒトアストロサイトへの感染
・270倍希釈したレンチウイルス(MOI=4.3)を感染
・感染3日後:ZsGreen1 陽性率95.7% -
-
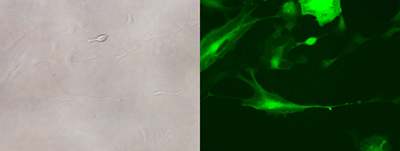
C)ラット脳皮質アストロサイトへの感染
・270倍希釈したレンチウイルス(MOI=4.3)を感染
・感染3日後:ZsGreen1 陽性率90.6%
ZsGreen1遺伝子を挿入したpLVSIN-CMV Pur VectorとLentiviral High Titer Packaging Mixを組み合わせて取得したZsGreen1発現レンチウイルスベクター上清を、各標的細胞への感染に使用した。感染にはRetroNectinを使用し、RBV-Spin法で行った。
この組み合わせで得たレンチウイルス上清は、多くの場合、濃縮しないで直接、標的細胞への感染に使用できる。

図2. EF1αプロモーターとCMVプロモーターの発現強度の比較(1 copy/cellでの相対値)
ZsGreen1遺伝子を挿入したpLVSIN-CMV PurまたはpLVSIN-EF1α Purベクターと、クロンテックLenti-X HTX Packaging System、Lenti-X 293T細胞を用いて組換えレンチウイルスを調製した。ウイルス上清の段階希釈液を用い、ポリブレン法、あるいはRetroNectin法で各細胞への感染を行い、2~3日後にフローサイトメーターを用いて遺伝子導入効率ならびにZsGreen1発現強度を測定した。遺伝子導入効率が20%以下のサンプルをsingle copy導入細胞とみなし、CMVプロモーターとEF1αプロモーターの発現強度を比較した。グラフではCMVプロモーターの発現強度を1とした場合の相対値を示している。
保存
-20℃
形状
| 10 mM | Tris-HCl (pH8.0) |
| 1 mM | EDTA |
ベクターマップ
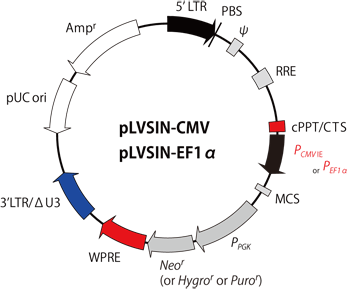
| ベクター | 鎖長 | 利用可能な制限酵素サイト(MCS) |
| pLVSIN-CMV Neo | 7,809 bp | EcoR I, Xho I, Xba I, Not I, BamH I |
| pLVSIN-CMV Hyg | 8,049 bp | Xho I, Xba I, Not I, BamH I |
| pLVSIN-CMV Pur | 7,614 bp | EcoR I, Xho I, Xba I, Not I, BamH I |
| pLVSIN-EF1α Neo | 8,386 bp | Sse8387 I, Smi I, Xba I, Not I, BamH I |
| pLVSIN-EF1α Hyg | 8,626 bp | Sse8387 I, Smi I, Xba I, Not I, BamH I |
| pLVSIN-EF1α Pur | 8,191 bp | Sse8387 I, Smi I, Xba I, Not I, BamH I |
DNAのシーケンスデータ
ZIP形式で圧縮しておりますが、StuffIt Expander等でも解凍できます。
使用上の注意
- 本製品の使用には遺伝子工学と細胞培養に関する基本的な技術が必要です。
- 本製品の使用には文部科学省の定める省令(「研究開発等に係る遺伝子組換え生物等の第二種使用等に当たって執るべき拡散防止措置等を定める省令」平成16年文部科学省・環境省令第1号)にあるP2レベル以上の施設が必要です。(→説明書の「バイオセーフティーについて」を参照してください。)
- 本レンチウイルスベクターの系によって生産されるウイルス上清は、挿入断片によっては危険なウイルスを含む恐れがあるため、組換えレンチウイルスの生産と取扱いには、適切な処置をとる必要があります。吸入や付着を防ぐため、必ず、安全キャビネットを使用してください。
- 本製品の使用はすべて研究用に限定されています。臨床目的での使用および生体外診断に使用することはできません。
- 本製品ご利用の際は省令および組織内の組換えDNA安全委員会の指示に従い、安全には十分ご注意下さい。
- 本製品の使用によって生じたいかなる事故、損害についても、弊社では責任を負いかねますので、ご了承の上ご使用下さい。
関連資料
関連のオンラインガイドはこちら
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。