製品説明
RetroNectinはインテグリンVLA-4、VLA-5を発現している哺乳類細胞に対してレトロウイルスベクター*2を介した遺伝子導入を行う際に有用である。VLA-4を発現している細胞はCS-1部位と、またVLA-5を発現している細胞は細胞接着ドメイン(RGDS 配列)と接着し、一方、ウイルスベクターはヘパリン結合ドメイン(Type III repeat, 12, 13, 14)に結合することによってRetroNectin上に共配置される。これにより、局所的に両者の濃度が高められ、遺伝子導入が促進されると考えられる(図1)。
*1 分子量62,613(アミノ酸配列より)
*2 レンチウイルスベクターを介した遺伝子導入を行う際にも有用です。
RetroNectin Dishは、RetroNectinを35 mm dishにあらかじめコーティングしたものである。コーティング操作が不要となり、一定の遺伝子導入効率を得ることができる。

図1.フィブロネクチンとレトロネクチンの構造およびレトロネクチンでの遺伝子導入のモデル図
標的細胞には(1)Supernatant法、または(2)RBV(RetroNectin-bound virus)法により遺伝子を導入する。
(1)Supernatant法
細胞とウイルスを混合してRetroNectinコートプレート上で感染させる方法である。簡便に短時間でRetroNectinを用いたウイルスベクターによる遺伝子導入を行うことができる。(図2)

図2.Supernatant法
(2)RBV法(改良法)
組換えレトロウイルスを先にRetroNectinコートプレートに吸着させ、感染阻害物質を含むレトロウイルス液を除いた後に細胞を加える方法である。RBV法はレトロウイルスベクターを介した遺伝子導入を行う際に、プロデューサー細胞から分泌されるプロテオグリカンやレトロウイルス包膜タンパク質などの物質が存在すると導入効率に影響を与えるため、組換えレトロウイルスを感染させるときにはこれらの阻害物質を除いておくことが重要であることから改良された方法である。Supernatant法で十分な遺伝子導入効率が得られない場合、RBV法を用いることを推奨する。特に、高濃度にウイルス液を使用する場合、より高い効果を発揮する。(図3)
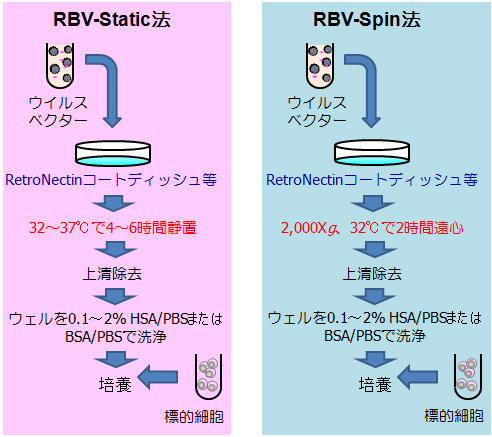
図3.RBV法
培養バッグを用いたラージスケールのウイルス感染方法(RBV-LTS法)の詳細はこちら。
さらに、RetroNectinはTリンパ球の培養を増強する効果も有する。
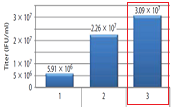
T細胞の拡大培養は、通常、抗CD3抗体刺激によりインターロイキン-2(IL-2)の存在下で行う。このときRetroNectinを共存させることで拡大培養効率が格段に増大する(実験例参照)。また、得られたT細胞集団中には未分化な細胞であるナイーブT細胞が多く含まれる。ナイーブT細胞は、抗原提示を受け細胞傷害性T細胞に分化する能力をもつ。
使用例
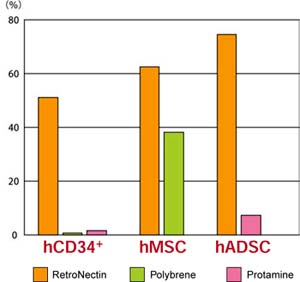
図4.レトロウイルスベクターを用いた3種類の幹細胞への遺伝子導入例
蛍光タンパク質発現レトロウイルスベクターをRetroNectin法、Polybrene法、Protamine法を用いて各細胞に遺伝子導入した。
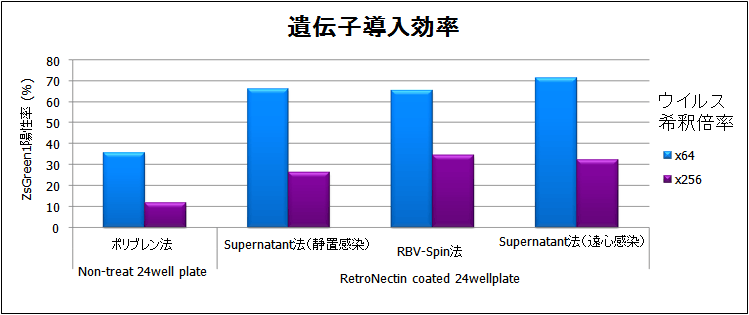
図5.レンチウイルスベクターを用いた浮遊系培養細胞(SUP-T1)への遺伝子導入例
蛍光タンパク質発現レンチウイルスベクターをSupernatant法(静置感染/遠心感染)、RBV-Spin法、Polybrene法を用いて各細胞に遺伝子導入した。
ラーニングビデオ
内容
RetroNectin 2.5 mg(2.5 ml)(製品コード T100B)
本製品は溶液品(ろ過滅菌処理済)(1 mg/ml)である。
(形状)12.5 mM クエン酸ナトリウム(pH6.2)、1.25% ショ糖(Sucrose)
保存
| 製品コード T100A、T100B | -20℃ |
| 製品コード T110A | 4℃ |
起源
濃度
1 μg/μl
分子量
純度
使用上の注意
- 本製品の凍結融解は10回程度まで可能である。
- 本製品の撹拌はゆるやかに行ってください。ボルテックスによる撹拌は避けてください。
プレートへのコーティング
プロトコルの詳細はこちら
関連のオンラインガイドはこちら
タカラバイオで展開している幹細胞研究のための試薬・受託サービス選択ガイドの他、関連情報をまとめています。
Protocols
RetroNectin®コートプレートの作製
RetroNectin Bound Virus(RBV)-Static法(静置感染)
RetroNectin Bound Virus(RBV)-Spin法(遠心感染)
Supernatant法(静置感染)
Supernatant法(遠心感染)
RetroNectin Bound Virus(RBV)-LTS法
Application
レンチウイルスベクターを用いた遺伝子導入方法の比較
RetroNectinを用いた造血系細胞への遺伝子導入
RetroNectinを用いた株化された培養細胞への遺伝子導入
ヒトCD34+造血幹細胞への遺伝子導入
3種類の幹細胞への遺伝子導入例
(レトロネクチン法、ポリブレン法、プロタミン法の比較)
正常ヒト神経前駆細胞への遺伝子導入
浮遊系培養細胞(SUP-T1)への遺伝子導入
レトロネクチン®共刺激によるTリンパ球(T細胞)拡大培養
各種初代培養細胞への感染
BIO VIEW / Clontechniques
RetroNectin®を用いた遺伝子導入法の最適化
Improve Viral Transductions with RetroNectin® Reagent
幹細胞・再生医療研究ガイド
タカラバイオで展開している幹細胞研究のための試薬・受託サービス選択ガイドの他、関連情報をまとめています
製品選択ガイド(組換えレトロウイルス関連)
使用文献・参考文献
関連製品・受託
RetroNectin® Dish
RetroNectin® GMP grade
pDON-5 DNA
pDON-AI-2 DNA
pMEI-5 DNA
pSINsiベクターシリーズ
pSINsi-DKベクターシリーズ
Retrovirus Packaging Kit
pLVSIN蛍光タンパク質ベクター
神経幹細胞維持/神経分化培地 RHB-A®
ヒト間葉系幹細胞(Mesenchymal Stem Cells:MSC)
ヒトCD34+ 前駆細胞(CD34+ Progenitor Cells)
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。