FFPEからTCR/BCRシーケンス用ライブラリーが作製可能
- イルミナ社次世代シーケンサー用ヒトT細胞受容体(TCR)、B細胞受容体(BCR)のレパトア解析ライブラリー調製キット
- FFPEサンプルなど低品質RNA(RIN≧4、DV200≧40%)に対応し、幅広いインプット量(200 ng~1 μg)で使用可能
- CDR3領域をターゲットとしたRT-PCRにより、すべてのヒトTCR鎖およびBCR鎖(TRA、TRB、TRG、TRD、IgG、IgM、IgA、IgD、IgE、IgK、IgL)を検出可能
- 1キットでヒトTCR、BCRの全鎖を網羅したライブラリーが作製可能、プライマーの選択によりTCR、BCR、個別のライブラリーも作製可能
- 分子バーコード(Unique Molecular Identifier : UMI)の利用により、PCRによるバイアスやシーケンスエラーを除去でき、希少なクロノタイプや重要な変異の同定の精度と信頼性が向上
- Unique Dual Index(UDI)の利用により、 最大96サンプルのマルチプレックス解析に対応でき、シーケンスコストを低減
- 分子バーコード(UMI)やUnique Dual Indexの利用で、より正確なNGS解析が可能
製品説明
MaxiSeq Human FFPE TCR+BCR(with UMIs)は、FFPEサンプルから抽出した200 ng~1 μgのRNAを用いて、T細胞受容体(TCR)およびB細胞受容体(BCR)のレパトア解析に必要なシーケンス用ライブラリーを調製できます。
本製品は、わずか200 ngの低品質RNA(RIN≧4、DV200≧40%)から、ヒトTCR鎖(TRA、TRB、TRG、TRD)、BCR重鎖(IgG、IgM、IgA、IgD、IgE)、軽鎖(IgK、IgL)のCDR3領域の配列を網羅的に取得します。TCR鎖とBCR鎖は、1つのライブラリーとして同時に解析することも、別々のライブラリーとして解析することも可能です。
さらに、UMIを使用することで、PCRによるバイアスやシーケンスエラーを除去し、希少なクロノタイプや重要な変異の検出精度が向上しています。
また、本製品にはUnique Dual Index(UDI)プレートが含まれており、最大96サンプルのマルチプレックスライブラリーを作製可能です。作製したライブラリーは、イルミナ社次世代シーケンサーのillumina NextSeq 500/550、NextSeq 2000、NovaSeqなどのプラットフォームに対応しています。
本製品は、わずか200 ngの低品質RNA(RIN≧4、DV200≧40%)から、ヒトTCR鎖(TRA、TRB、TRG、TRD)、BCR重鎖(IgG、IgM、IgA、IgD、IgE)、軽鎖(IgK、IgL)のCDR3領域の配列を網羅的に取得します。TCR鎖とBCR鎖は、1つのライブラリーとして同時に解析することも、別々のライブラリーとして解析することも可能です。
さらに、UMIを使用することで、PCRによるバイアスやシーケンスエラーを除去し、希少なクロノタイプや重要な変異の検出精度が向上しています。
また、本製品にはUnique Dual Index(UDI)プレートが含まれており、最大96サンプルのマルチプレックスライブラリーを作製可能です。作製したライブラリーは、イルミナ社次世代シーケンサーのillumina NextSeq 500/550、NextSeq 2000、NovaSeqなどのプラットフォームに対応しています。
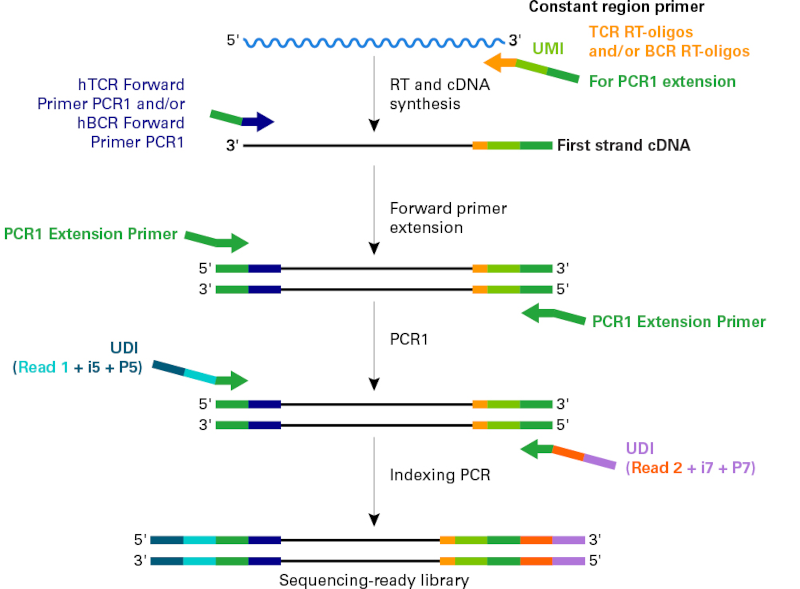
図1.MaxiSeq Human FFPE TCR+BCR(with UMIs)の原理とワークフロー
本製品は、遺伝子特異的プライマーを用いたRT-PCR法によってT細胞受容体(TCR:α、β、γ、δ)およびB細胞受容体(BCR:IGH、IGK、IGL)のCDR3領域の配列を効率的に取得できる。逆転写プライマーとしてUMIが組み込まれた遺伝子特異的プライマーを用いており、逆転写時にUMIを組み込むことにより、PCRによるバイアスを除去し、クロノタイプの正確なカウントが可能となる。
SMART-Seq Human TCR (with UMIs)などの免疫レパトア解析用のSMART-Seqキットが完全長のV(D)J領域を取得するために5’ RACE法を応用しているのに対し、本製品はCDR3領域をターゲットとするRT-PCR法を採用しており、分解が進んだRNAサンプルからのレパトア解析に適している。
本製品のワークフローは、まずTCR、BCRに特異的なプライマーを用いて、mRNAからFirst strand cDNAを合成しCDR3領域を増幅する(PCR1)。続いて、PCR1で増幅した産物の一部を用いたIndexing PCR(PCR2)によってインデックス(UDI)を付加したライブラリーを作製する。
本キットで作製したライブラリーは、サイズセレクションを兼ねた精製、品質確認後にシーケンスに使用することができる。
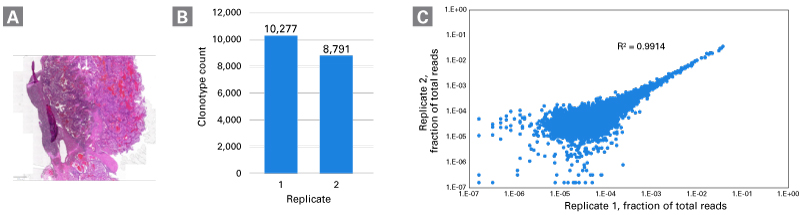
図2.腎細胞がんFFPE組織からの高品質な免疫プロファイリングライブラリー調製
MaxiSeq Human FFPE TCR+BCR(with UMIs)を用いて、RNA分解が進んだ腎細胞がんのFFPE組織から、免疫プロファイリングライブラリーを作製し、シーケンス解析を実施した。
パネルA:腎細胞がんFFPE組織のH&E染色像
パネルB:腎細胞がんFFPE組織から検出されたTCRクロノタイプ
パネルC:レプリケートを用いた再現性の確認(RNAインプット量:200 ng)
分解が進んだFFPEサンプルから再現性の高い結果が得られており(パネルC)、本キットを用いて信頼性の高い免疫プロファイリングが可能であることが示された。
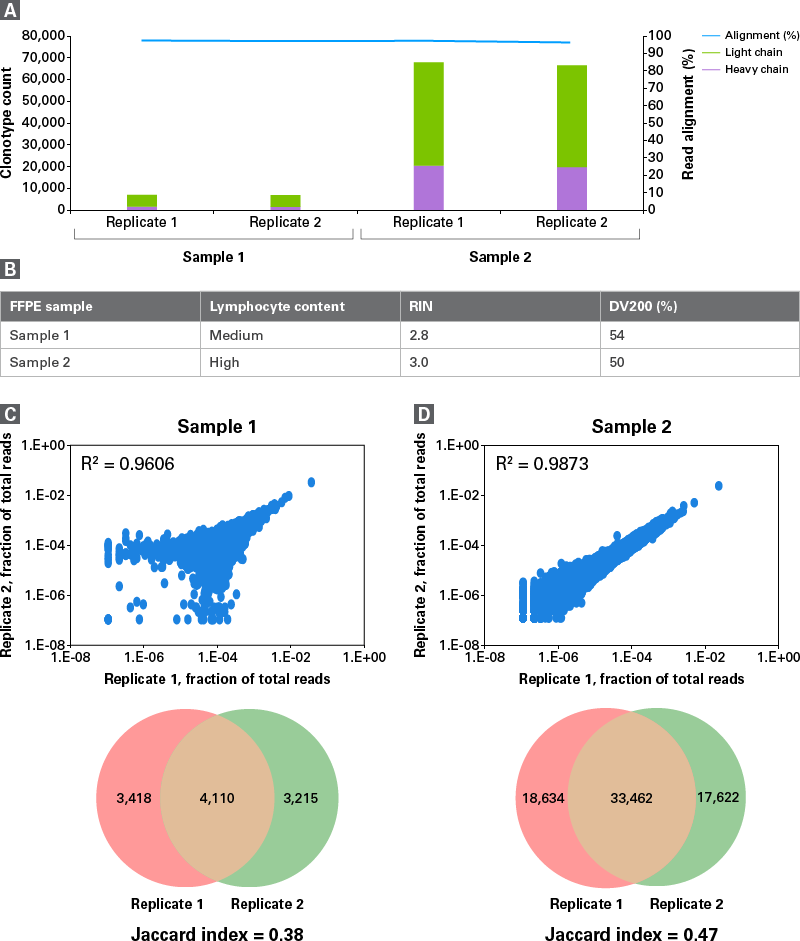
図3. 腫瘍浸潤リンパ球(TIL)FFPEサンプルにおけるBCRクロノタイプの高再現性プロファイリング
MaxiSeq Human FFPE TCR+BCR(with UMIs)を用いて、異なる2種類の腫瘍浸潤リンパ球(TIL)FFPEサンプルからBCRライブラリーをレプリケートで調製し、クロノタイプを解析した。
パネルA:各サンプルで検出されたBCRクロノタイプカウント
パネルB:各サンプルのリンパ球含量とRNAの分解度
パネルC:各サンプルにおけるレプリケート間の相関性(R2>0.96)
パネルD:各サンプルにおけるレプリケート間の重複度(Jaccard指数0.33~0.47)
2種類のTIL FFPEサンプルをレプリケートで解析した結果、Sample2では、より多くのBCRクロノタイプが検出されおり、Sample1に比べてリンパ球の含有量が高いためと考えられる(パネルA、B)。
それぞれ、レプリケート間で高い再現性が示されており、相関係数(R2)は0.96以上となった(パネルC)。一方、レプリケート間の重複度は低く、クロノタイプの多様性が示された(パネルD)。
内容
- MaxiSeq Human FFPE TCR+BCR (with UMIs)(製品コード 634386/634387)
-
Package 1
Human PBMC RNA (50 ng/μl)
Package 2
TCR RT-Oligos (20X)
BCR RT-Oligos (20X)
hTCR Forward Primer PCR1 (20X)
hBCR Forward Primer PCR1 (20X)
Binding Buffer (4X)
Nuclease-Free Water
dNTPs (10 mM)
RT Buffer (5X)
Reverse Transcriptase (20X)
RT Extension Oligos (20X)
PCR Buffer (5X)
DNA Polymerase (100X)
PCR1 Extension Primer (10X)
Exonuclease
Forward Sequencing Primer (100 μM)
Reverse Sequencing Primer (100 μM)
Forward Indexing Primer (100 μM)
Reverse Indexing Primer (100 μM)
Package 3
MaxiSeq Human FFPE TCR+BCR (with UMIs) Unique Dual Index Plate
保存
Package 1:-70℃
Package 2:-20℃
Package 3:-20℃
Package 2:-20℃
Package 3:-20℃
本製品以外に必要な試薬、機器(主なもの)
- シングルチャンネルピペット:10 μl、20 μl、200 μl
- 8チャンネルピペット(推奨):20 μl、200 μl
- フィルター付きピペットチップ:2 μl、20 μl、200 μl
- 透明接着フィルム(96ウェルプレート用)
- 微量遠心機
PCR増幅およびバリデーション
- 1st strand cDNA合成専用のPCRサーマルサイクラー
- PCR amplification用のPCRサーマルサイクラー
- Agilent 2100 Bioanalyzer:High Sensitivity DNA Kit(Agilent社、Cat. No.5067-4626)、またはFragment Analyzer(NGS Fragment Kit(1-6000 bp)、Agilent、Cat. No.DNF-473-1000)、Agilent 4150/4200 TapeStation(High Sensitivity D5000 ScreenTape(Cat. No.5067-5592)、High Sensitivity D1000 ScreenTape(Cat. No.5067-5584))
- Qubit dsDNA HS Assay Kit(Thermo Fisher Scientific社、Cat. No.Q32851)
- Nuclease-free thin-wall PCR tube、または96-well nuclease-free thin-wall PCR plate、もしくは strips
- 1.5 ml低吸着マイクロ遠心チューブ
SPRI Bead精製
- NucleoMag NGS Clean-up and Size Select(製品コード 744970.5/.50/.500)
※NucleoMagの代わりにAMPure XP PCR purification kit(Beckman Coulter社; 5 ml size: code. A63880; 60 ml size: code.A63881)も使用可能 - 100%エタノール(molecular biology grade)
- マグネットスタンド
- 96ウェルVボトムプレート(500 μl;VWR社、Cat. No.47743-996)
- MicroAmp Clean Adhesive Film(Thermo Fisher Scientific社、Cat. No.4306311)
- 96ウェルプレート用卓上低速遠心分離機
この製品を見た人は、
こんな製品も見ています
-

Trekker® Single-Cell Spatial Mapping Kit
真のシングルセル空間トランスクリプトーム解析用試薬
-
Cellartis® MSC EV Wonder™
ヒト間葉系幹細胞からの細胞外小胞産生を誘導
-
NucleoSpin® 96 RNA Plant and Fungi
植物および糸状菌サンプルからtotal RNAをハイスループット精製
-
Seeker™ Spatial Transcriptomics Kit
専用装置不要の全トランスクリプトーム空間解析用試薬
-
TaKaRa腸管系病原細菌遺伝子検出キットVer.5
qPCR/融解曲線分析による検便検査キット(EHEC、サルモネラ、赤痢菌)
-
モリナガ 甲殻類キットII
消費者庁通知準拠のえび・かに用の特定原材料検査キット
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。

