遺伝子・細胞プロセッシングセンター CGCP(Center for Gene and Cell Processing)
タカラバイオでは、大規模GMP/GCTP対応施設 CGCP(Center for Gene and Cell Processing)において、再生医療等製品やバイオ医薬品の開発・製造を行っています。製造能力を増強するとともに製造品目を拡大して、多様なモダリティに対応しています。再生医療等製品製造業許可および医薬品製造業(生物学的製剤等)許可のもと、プロセス開発、治験製品製造に加え、商用生産に至るまで、お客様の様々なニーズに対してトータルでサポートいたします。
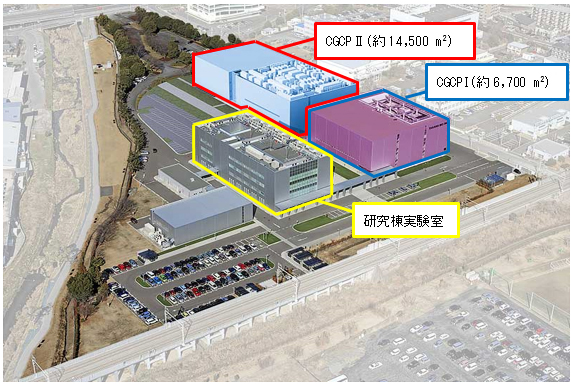
CGCP I & CGCP II(滋賀県草津市)
- ■概要
-
大規模GMP/GCTP対応施設 CGCP(Center for Gene and Cell Processing)では、再生医療等製品に特化し、各種セルバンク、DNA/RNAワクチン、遺伝子治療用ウイルスベクターおよび細胞製剤を、GMP/GCTPに準拠して製造しています。また、同施設内で品質試験や特性解析を行い、日本国内最大規模の“one-stop GMP manufacturing facility”として、お客様の臨床開発から上市後の商用生産までトータルでサポートいたします。

- ■特徴
-
- ISO9001および治験薬GMPに準拠して運用
2015年 5月に特定細胞加工物製造許可を取得(施設番号: FA5150002)
2019年 3月に再生医療等製品製造業許可を取得
2019年 5月に再生医療等製品製造販売業許可を取得
2020年 6月に医薬品製造業(許可区分:生物学的製剤等)許可を取得 - 各製造室に独立した空調システムを採用し、交差汚染によるコンタミネーションリスクを最小化
- エアロックシステムを応用し、製造室における組換え体の封じ込めと外部からの汚染リスクを最小化
- 同一施設内に複数の製造室を設け、同時に多品目の製造を実現
- 原料/製品保管庫や品質試験エリアを施設内に設け、効率の良い製造作業を実現
- 製造エリアへの作業者や原料等の流れを別にし、一方通行により交差汚染のリスクを最小化
- ISO9001および治験薬GMPに準拠して運用
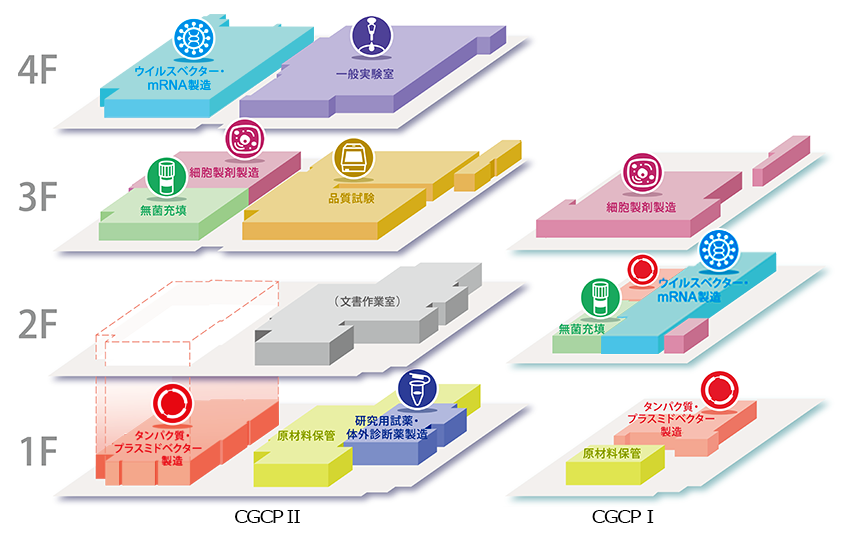
ウイルスベクター製造
◆世界トップレベルの大量製造ラインを設置
(浮遊培養 最大2,000 L、接着培養 最大500 m2)
◆商用スケールの製造体制を整備
mRNA製造
◆5 g以上のラージスケールのmRNA製造
◆最新の機器を取り揃え、様々な精製が可能

一般試験室
◆各品目の基礎研究からプロセス開発を実施
◆スケーラビリティーを持つ機器を複数台設置し、製法を最適化

細胞製剤製造
◆複数台のアイソレーターや閉鎖系自動培養装置を備え、高い無菌性を保証
◆他家の細胞製剤に対応可能なスケールで製造

無菌充填
◆製造した原薬等は本施設内で迅速に無菌充填室で製剤化が可能
◆最大3,600本/時 自動充填で実施可能
◆全数充填重量管理を実施


細胞製剤製造
◆シングルユースの培養器材を活用し、多品種の培養に対応
◆11室の細胞加工室を整備
◆iPS細胞を含むヒト由来細胞のセル・バンクや、遺伝子改変T細胞などの細胞製剤など目的に合わせた製造プロセスの構築、製造が可能

無菌充填
◆アイソレーターやRABS内の低温(2~10℃)管理下での充填が可能
◆無菌ろ過フィルターの使用前完全性試験も対応
◆外観異物検査、表示、包装までの工程が実施可能
タンパク質・プラスミドベクター製造
◆2,000 Lのマルチユースバイオリアクターによるラージスケール製造
◆連続遠心分離機や大型精製装置も設置して、高純度なプラスミドを製造


タンパク質・プラスミドベクター製造
◆グラムスケールのプラスミドDNAのGMP製造
◆25~200 Lまでのシングルユースバイオリアクターによる製造
◆独自の高密度培養技術や閉鎖系システムによる高品質な製造

品質試験
◆製造と同施設内で品質試験や特性解析を実施
◆約1,750 m2のスペースに無菌・マイコプラズマ試験、細胞・ウイルス試験、PCR試験など各試験ごとにエリアを設置
◆細胞・ウイルス試験エリアは、室間差圧によるハザード封じ込め管理を行い、あらゆる検体の取り扱いが可能


ウイルスベクター製造
◆多段式フラスコや浮遊培養装置を用いた開発初期の小スケール製造から対応
◆これまで培ってきた製造ノウハウを活かし、多様なウイルス種・スケールでの実績
◆バイアルやバッグなどへの無菌充填ラインを整備
mRNA製造
◆2022年にmRNA原薬製造ラインを立ち上げ、複数の治験薬を製造
◆約1 g程度のmRNA製造に対応
◆様々な製法やスケールに柔軟に対応
ファシリティ・オブ・ザ・イヤー受賞
ファシリティ・オブ・ザ・イヤーは2005年に設立され、優れた革新的な技術によって設計、建設、運営されている医薬品や医療機器の製造・開発施設に授与されます。タカラバイオの遺伝子・細胞プロセッシングセンターが受賞したファシリティ・インテグレーション部門賞は6つある部門賞の1つで、CDMO事業において求められる、多品目の再生医療等製品等を安全かつ効率的に製造できる施設として、設計、運営、環境等の面で調和がとれている点が評価され、受賞に至りました。

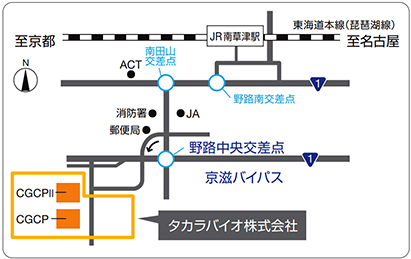
アクセス
|
<遺伝子・細胞プロセッシングセンター(CGCP)> 滋賀県草津市野路東7丁目4番38号 ・交通手段 南草津駅よりタクシー 約10分 |
|
- 注意事項
- 本受託サービスは、個別に合意した場合を除き、すべて研究目的として作業を行います。納品物を試験研究目的以外へご使用される場合、弊社では納品物に起因する損失・損害等については一切の責任を負いかねます。納品物によっては、その構成物(例えば、ベクター、蛍光色素など)の使用に制限がある場合がありますのでご注意ください。
- 納品物に起因して、直接的もしくは間接的に発生したお客様の損害については、明らかに弊社の責に帰すべき事由による場合を除いて、弊社は一切その責任を負いません。
- ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。









