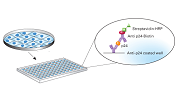
サンプルのお申し込みはこちらから
- スマートフォンのアプリを使用して10分間でレンチウイルス量の測定が可能
- レンチウイルス回収の最適なタイミングを判断
- ウイルス量を測定することにより、一貫性のある実験が可能

実験アンケート結果
製品説明
Lenti-X GoStix Appでの定量的な判定(GoStix Value、GV)は、ELISAよりはるかに簡単で迅速な方法で、異なるウイルスの力価を比較することがきる。また、あらかじめ感染力価が既知の標準ウイルスを用いてGVとIFU/mlへの換算値を求めておけば、未知サンプルのIFU/mlを計算することも可能である。
Lenti-X GoStix Plusを使用すると、迅速かつ簡単にレンチウイルス量の測定を行うことができるので、レンチウイルス導入時のばらつきを最小限に抑え、一貫したパフォーマンスで実験することが可能である。
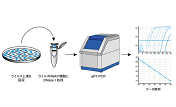
Lenti-X GoStix Plusによるレンチウイルス量の測定では、Lenti-X GoStixアプリでGoStixカセットをスキャンし、テストバンドとコントロールバンドの画像を取り込み、各バンドの強度を測定して計算した結果をGoStix Value (GV)として表示します。
ELISA法で測定されたp24タンパク質量やqPCRで測定されたウイルスゲノムのコピー数は、その結果が感染力価と相関することが知られています。同じ様に、GVも感染力価と相関します。
なお、ウイルス力価(IFU/ml)を求めるには、あらかじめ感染力価が既知の標準ウイルスを用いてGVからIFU/mlへの換算値を求めておくことが必要です。
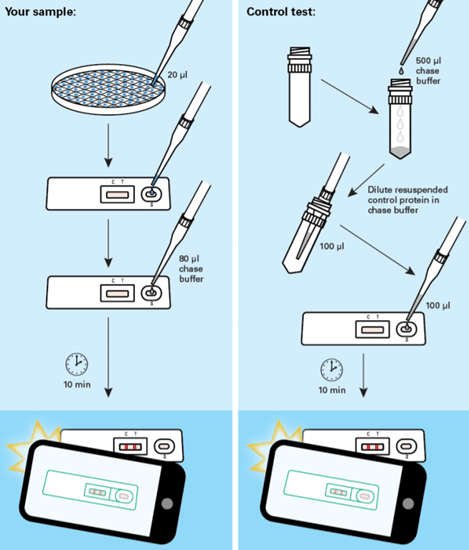
パッケージング細胞の培養上清中に十分なウイルスが含まれ、回収・精製に適している場合、GoStix Plusのテストバンドに明瞭なラインが現れる。スマートフォンが無い場合、5×105 IFU/ml*以上の力価を定性検出できる。
* IFU:ウイルス力価はHT1080細胞に感染させフローサイトメーターで測定
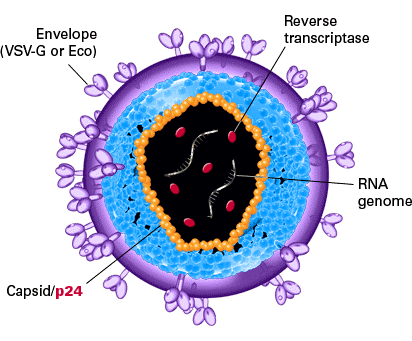
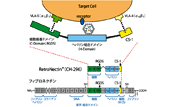
p24タンパク質はレンチウイルスキャプシドを構成する4つのタンパク質の一種で、HIV-1 gag遺伝子にコードされている。パッケージング細胞上清中に存在するp24の量を定量することにより、レンチウイルス力価を測定することができる。
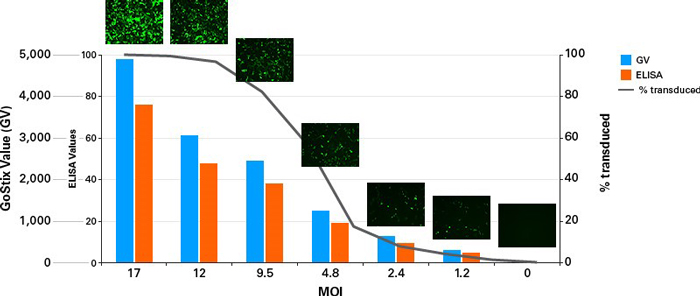
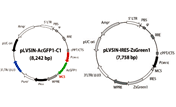
Lenti-X Packaging Single Shotsレンチウイルスパッケージングシステムを用いてZsGreen1発現レンチウイルスを作製し、HT1080細胞にウイルスを感染させ、フローサイトメーターによってウイルス感染効率(%)を調べた。また、Lenti-X p24 Rapid Titer Kitを用いてウイルスp24値を、Lenti-X GoStix Plusを用いて GoStix Valueをそれぞれ調べた。HT1080感染のM.O.I.と感染効率をプロットし、それに対するELISAおよびGoStix Valueの結果の同等性を検証した。蛍光顕微鏡の写真は感染48時間後の細胞の様子を示している。
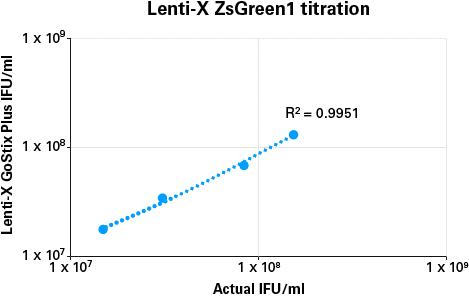
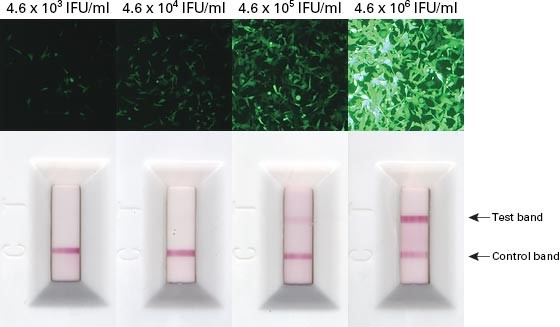
Lenti-X Packaging Single Shotsレンチウイルスパッケージングシステムを用いてZsGreen1発現レンチウイルスを作製し、得られたウイルスサンプルを段階希釈した。各希釈サンプルをLenti-X GoStix Plusカセットに添加して解析を行った。また、各希釈サンプルをHT1080細胞に感染させてIFU/mlの測定を行った。予めテストサンプルと同じパッケージングシステム、同じ培養時間によって作製した標準ウイルスを用いてGVからIFU/mlへの換算率を求めておき、段階希釈サンプルのGVからウイルス力価(IFU/ml)を算出した。
Lenti-X GoStix Plusの結果から計算したIFU/mlを実際に細胞に感染させて測定したIFU/mlとの相関性を示した。
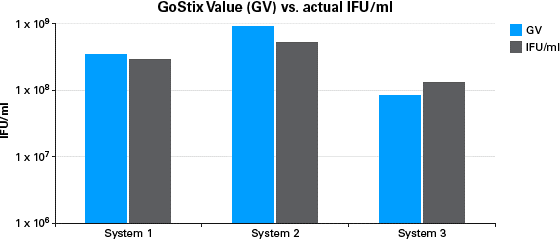
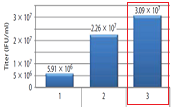
市販の3種類のレンチウイルスベクターおよびパッケージングシステムを用いてZsGreen1発現レンチウイルスを作製した。それぞれのウイルスサンプルを希釈し、Lenti-X GoStix Plusカセットに添加し、解析を行った。 また、それぞれの希釈サンプルをHT1080細胞に感染させ、正確なタイター(IFU/ml)を測定した。 予めテストサンプルと同じパッケージングシステム、同じ培養時間によって作製した標準ウイルスを用いてGVからIFU/mlへの換算率を求めておき、それぞれの希釈サンプルのGVからウイルス力価(IFU/ml)を算出した。
内容
- Lenti-X GoStix Plus(製品コード 631281 50回用)
-
・Lenti-X GoStix Plus50個
・Chase Buffer (3 ml/vial)4 vials
・p24 Control (5 tests/vial)1 vial
保存
p24 Controlは、1 vialにChase Bufferを24滴加えて(~500 μl)溶解する。溶解後のp24 Control溶液は4℃で保存する。長期保存する場合は、0.1%アジ化ナトリウムを加えて4℃で保存する。
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。