※仕様変更のお知らせ
RetroNectin GMP grade(製品コード T202)につきまして、2025年2月より仕様の一部を変更いたしました。
該当ロットや変更の詳細についてはお問い合わせください。
本製品は、専用発注書にてお申し込みください。RetroNectin GMP grade(製品コード T202)につきまして、2025年2月より仕様の一部を変更いたしました。
該当ロットや変更の詳細についてはお問い合わせください。
なお、発送に関しては下記2種類から選択していただけます。
- 販売店経由
弊社販売店からお届けいたします。(輸送費無料) - 直送(輸送時の温度モニタリングを希望される場合、専用発注書にてお申し込みください。)
※温度モニタリングサービス付き輸送について:
2026年3月より、温度モニタリングサービスに関して、お客様ご自身で輸送業者にお申し込みいただく手続きへ変更いたしました。
輸送業者へのお申し込み時に必要となる事項(弊社からの出荷日や荷姿など)は弊社からご案内します。
詳しくはお問い合わせください。
製品説明
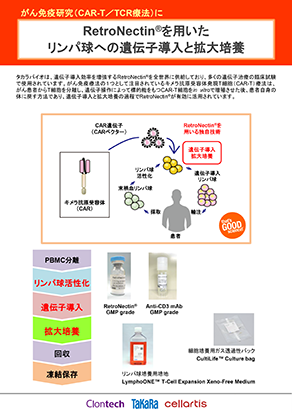
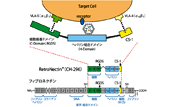
RetroNectin(リコンビナントヒトフィブロネクチンCH-296)1)は、ヒトフィブロネクチンの細胞接着ドメイン(C-domain)、ヘパリン結合ドメイン(H-domain)およびCS-1部位の3種類の機能性ドメインを含む組換えタンパク質である。
RetroNectinはインテグリンVLA-4、VLA-5を発現している哺乳類細胞に対してレトロウイルスベクター*1を介した遺伝子導入を行う際に有用である。VLA-4を発現している細胞はCS-1部位と、またVLA-5を発現している細胞は細胞接着ドメイン(RGDS 配列)と接着し、一方、ウイルスベクターはヘパリン結合ドメイン(Type III repeat, 12, 13, 14)に結合することによってRetroNectin上に共配置される。これにより、局所的に両者の濃度が高められ、遺伝子導入が促進されると考えられる(図1)。
タカラバイオでは、調製した組換えレトロウイルス液に含まれる感染阻害物質を除く方法を報告し、プロトコールの改良を行った2)。
レトロウイルスベクターを介した遺伝子導入を行う際に、プロデューサー細胞から分泌されるプロテオグリカンやレトロウイルス包膜タンパク質などの物質が存在すると導入効率に影響を与える。従って、組換えレトロウイルスを感染させる時にはこれらの阻害物質を除いておくことが重要である。
従来法*2(Supernatant感染法)では細胞とウイルスを混合してRetroNectinコートプレート上で感染させていたのに対し、改良法(RetroNectin-bound virus感染法)では組換えレトロウイルスを先にRetroNectinコートプレートに吸着させ、感染阻害物質を含むレトロウイルス液を除いた後に細胞を加え、感染させる。
RetroNectin法は、レトロウイルスベクターやレンチウイルスベクターを介する哺乳類細胞への遺伝子導入法として広く活用されている。
RetroNectin GMP gradeはGMPグレードのRetroNectinであり、PIC/S(医薬品査察協定及び医薬品査察共同スキーム)のGMPガイドラインに準拠し、製造および品質管理されている。そのため、研究用として販売しているRetroNectin(製品コード T100A/B)より高品質であり、ex vivoでの遺伝子治療や細胞調製等の臨床研究に使用可能である。
また、本製品は2019年3月15日付で、米国食品医薬品局(Food and Drug Administration: FDA)のドラッグマスターファイル(Drug Master File: DMF)に登録されている(弊社ニュースリリース)。再生医療等製品などの製造に求められる組換えタンパク質として高い品質を担保している。

図1.フィブロネクチンとレトロネクチンの構造およびレトロネクチンでの遺伝子導入のモデル図
RetroNectinはインテグリンVLA-4、VLA-5を発現している哺乳類細胞に対してレトロウイルスベクター*1を介した遺伝子導入を行う際に有用である。VLA-4を発現している細胞はCS-1部位と、またVLA-5を発現している細胞は細胞接着ドメイン(RGDS 配列)と接着し、一方、ウイルスベクターはヘパリン結合ドメイン(Type III repeat, 12, 13, 14)に結合することによってRetroNectin上に共配置される。これにより、局所的に両者の濃度が高められ、遺伝子導入が促進されると考えられる(図1)。
タカラバイオでは、調製した組換えレトロウイルス液に含まれる感染阻害物質を除く方法を報告し、プロトコールの改良を行った2)。
レトロウイルスベクターを介した遺伝子導入を行う際に、プロデューサー細胞から分泌されるプロテオグリカンやレトロウイルス包膜タンパク質などの物質が存在すると導入効率に影響を与える。従って、組換えレトロウイルスを感染させる時にはこれらの阻害物質を除いておくことが重要である。
従来法*2(Supernatant感染法)では細胞とウイルスを混合してRetroNectinコートプレート上で感染させていたのに対し、改良法(RetroNectin-bound virus感染法)では組換えレトロウイルスを先にRetroNectinコートプレートに吸着させ、感染阻害物質を含むレトロウイルス液を除いた後に細胞を加え、感染させる。
RetroNectin法は、レトロウイルスベクターやレンチウイルスベクターを介する哺乳類細胞への遺伝子導入法として広く活用されている。
RetroNectin GMP gradeはGMPグレードのRetroNectinであり、PIC/S(医薬品査察協定及び医薬品査察共同スキーム)のGMPガイドラインに準拠し、製造および品質管理されている。そのため、研究用として販売しているRetroNectin(製品コード T100A/B)より高品質であり、ex vivoでの遺伝子治療や細胞調製等の臨床研究に使用可能である。
また、本製品は2019年3月15日付で、米国食品医薬品局(Food and Drug Administration: FDA)のドラッグマスターファイル(Drug Master File: DMF)に登録されている(弊社ニュースリリース)。再生医療等製品などの製造に求められる組換えタンパク質として高い品質を担保している。
| *1 | レンチウイルスベクターを介した遺伝子導入を行う際にも有用です。 |
| *2 | 従来法でも十分な遺伝子導入効率を得ることができます。 また、改良法は適応範囲の広い方法ですが、標的細胞、ベクター、目的遺伝子によって条件検討が必要な場合もあります。 |

図1.フィブロネクチンとレトロネクチンの構造およびレトロネクチンでの遺伝子導入のモデル図
ラーニングビデオ

RetroNectinを用いた遺伝子導入をビデオ(英語)で分かりやすくご紹介しています。
詳細はこちらをご確認ください。
保存
-30℃以下
起源
E. coli expressing human fibronectin fragment CH-296
形状
1 mg/ml、12.5 mMクエン酸ナトリウム・1.25%スクロース、pH6.2
包装形態
2.5 mg/2.5 mlのタンパク質溶液を5 mlのガラスバイアルで包装
分子量
62,617(アミノ酸配列より算出、574アミノ酸)
純度
HPLCにて純度90%以上
使用上の注意
・無菌的な環境下で作業してください。
・融解したRetroNectin溶液は室温放置で12時間以内に使用してください。
・一旦融解したRetroNectin溶液の後日の再利用は避けてください。
・融解したRetroNectin溶液は室温放置で12時間以内に使用してください。
・一旦融解したRetroNectin溶液の後日の再利用は避けてください。
品質について
- RetroNectin GMP gradeは、PIC/S(医薬品査察協定及び医薬品査察共同スキーム)のGMPガイドラインに準拠し、製造および品質管理されています。
- 本製品の製造工程には、ヒトおよび動物由来原料を使用しておりません。
- 本製品は米国FDA内CBER(Center for Biologics Evaluation and Research)のBiologics Master File (BB-MF) # 18898に登録されています。
備考
RetroNectin法は、レトロウイルスベクターやレンチウイルスベクターを介する哺乳類細胞への遺伝子導入法として広く活用されているが、さらに、Tリンパ球の培養を増強する効果が確認された。
T細胞の拡大培養は、通常、抗CD3抗体刺激によりインターロイキン-2(IL-2)の存在下で行う。このときRetroNectinを共存させることで拡大培養効率が格段に増大する(実験例参照)。また、得られたT細胞集団中には未分化な細胞であるナイーブT細胞が多く含まれる。ナイーブT細胞は、抗原提示を受け細胞傷害性T細胞に分化する能力をもつ。
T細胞の拡大培養は、通常、抗CD3抗体刺激によりインターロイキン-2(IL-2)の存在下で行う。このときRetroNectinを共存させることで拡大培養効率が格段に増大する(実験例参照)。また、得られたT細胞集団中には未分化な細胞であるナイーブT細胞が多く含まれる。ナイーブT細胞は、抗原提示を受け細胞傷害性T細胞に分化する能力をもつ。
Protocols
RetroNectin GMP gradeのフィルターろ過およびコーティング
G-Rex®×RetroNectin®×レンチウイルスベクターによるCAR-T細胞作製プロトコール
Application
RetroNectinを用いた造血系細胞への遺伝子導入
RetroNectinを用いた株化された培養細胞への遺伝子導入
ヒトCD34+造血幹細胞への遺伝子導入
3種類の幹細胞への遺伝子導入例
(レトロネクチン法、ポリブレン法、プロタミン法の比較)
レトロネクチン®共刺激によるTリンパ球(T細胞)拡大培養
BIO VIEW / Clontechniques
RetroNectin®を用いた遺伝子導入法の最適化
Improve Viral Transductions with RetroNectin® Reagent
この製品を見た人は、
こんな製品も見ています
-

CultiLife™ Culture bag
細胞培養用ガス透過性バッグ
-

G-Rex®(ガス透過性培養システム)
免疫細胞の大量培養に適した製造プラットホーム
-

Recombinant Cas9 Protein GMP grade
GMPグレードの組換え型Cas9タンパク質
-
RetroNectin® (Recombinant Human Fibronectin Fragment)
高効率遺伝子導入とリンパ球の拡大培養に
-

Anti-CD3 mAb GMP grade
GMPグレードの抗CD3モノクローナル抗体
-

RetroNectin® Pro (Recombinant Human Fibronectin Fragment)
リンパ球の遺伝子導入と拡大培養を低コストで効率的に!
- 注意事項
- 本ページの製品はすべて研究用として販売しております。商用生産用途にご利用いただく場合、事前のライセンス契約締結が必要です。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- 記載されている会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。