※試験項目等の概要はこちら
- 感染性因子に対する試験
mRNA医薬品の安全性を可能な限り高めるため、混入する恐れのある感染性因子のリスク評価に基づき、原材料、工程内中間体または最終製品の適切な段階で妥当な管理方法を設定する必要があります。タカラバイオではGMP管理体制の下、微生物試験や各種ウイルス試験をご提供します。
細胞および原材料等の安全性試験 - 純度試験
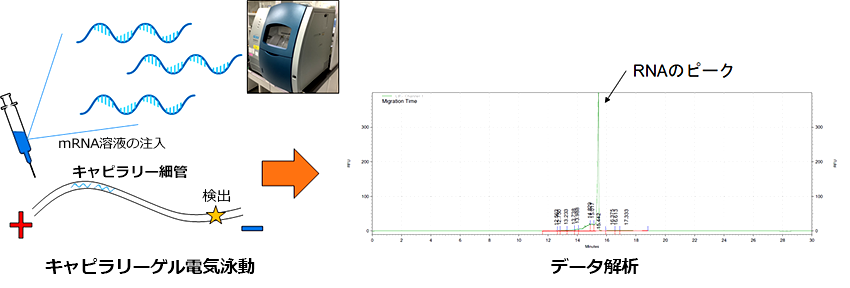
医薬品製造において製造工程由来不純物の除去は品質や安全性の担保に重要です。mRNA医薬品では、目的mRNA以外の夾雑物の含有量を明確にすることが推奨されます。試験例:mRNA完全性試験mRNAの製造工程において、不完全なmRNAが生成される場合があります。本試験では、目的の全長RNA含有率をキャピラリー電気泳動(CE)を用いて測定します。
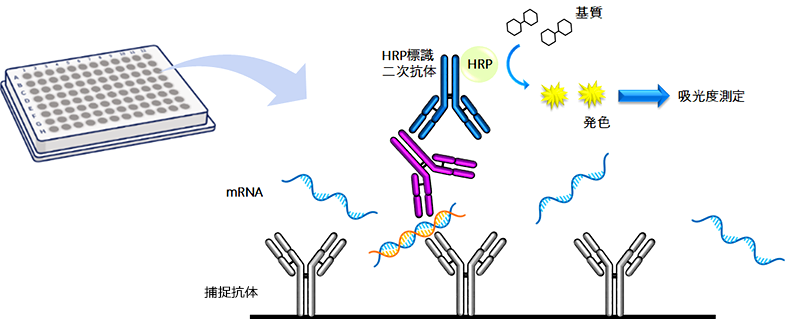
試験例:dsRNA残留試験二本鎖(ds)RNAはmRNA医薬品製造時の目的物質由来不純物であり、免疫原性の原因となりうることが指摘されています。本試験では、dsRNAを特異的に認識する抗体を用いたELISA法により、dsRNAを定量します。
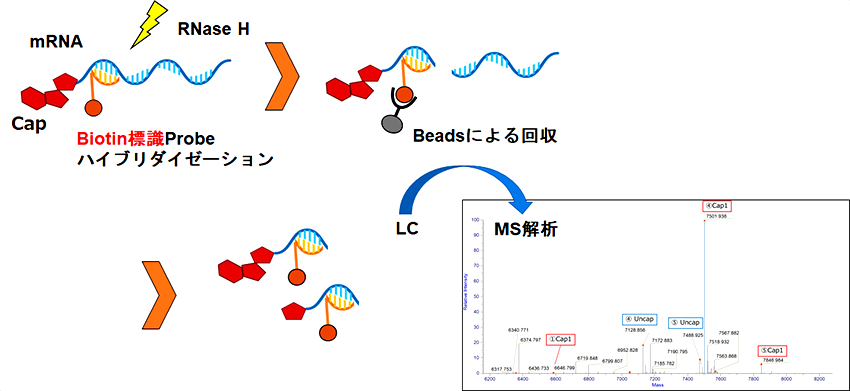
試験例:Capping効率試験mRNAの5’キャップ構造はmRNAの安定性や翻訳に重要とされています。また、その構造によりmRNAは細胞内免疫応答を回避します。本試験では、mRNAに相補的なプローブを結合させRNase Hにより切断し、5’末端領域のフラグメントをLC/MSを用いた質量分析により分析し、キャッピング効率を測定します。
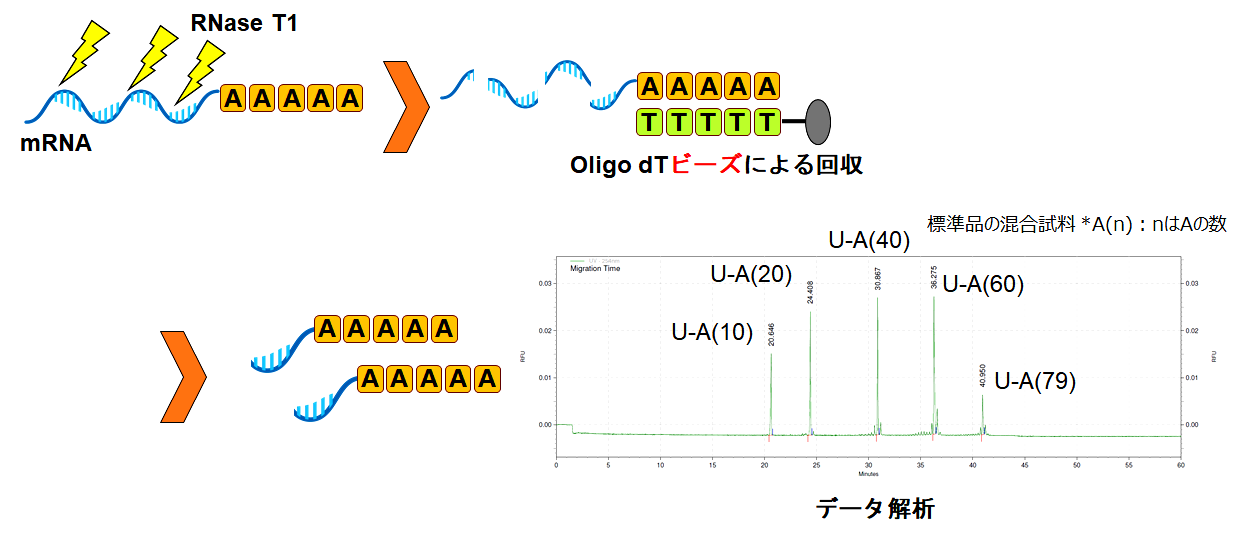
試験例:PolyA鎖長解析3’末端のPolyA鎖はmRNAの安定性と翻訳の調節に寄与することが知られています。本試験では、mRNAをRNaseT1により切断し、3’末端領域のフラグメントをキャピラリーゲル電気泳動(CE)を用いて分析し、PolyA鎖長を推定します。
- 安定性試験
各種ガイドラインにおいて、また使用期限・保管条件の設定のために、原薬および製剤の安定性試験の実施が求められます。開発段階および最終製品について、試験項目、試験ポイント、保存条件などをご相談の上決定いたします。
安定性試験 - 標準物質作製
医薬品の品質評価試験において、適切な標準物質は重要です。標準物質は各種品質試験のほか、試験に用いる装置の校正分析システムの適合性試験等に用います。各試験に適した信頼性の高い標準物質の作製・品質管理を承ります。
※その他試験詳細につきましてはお問い合わせください。
関連製品・受託
- 注意事項
- 本受託サービスは、個別に合意した場合を除き、すべて研究目的として作業を行います。納品物を試験研究目的以外へご使用される場合、弊社では納品物に起因する損失・損害等については一切の責任を負いかねます。納品物によっては、その構成物(例えば、ベクター、蛍光色素など)の使用に制限がある場合がありますのでご注意ください。
- 納品物に起因して、直接的もしくは間接的に発生したお客様の損害については、明らかに弊社の責に帰すべき事由による場合を除いて、弊社は一切その責任を負いません。
- ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。