アデノ随伴ウイルスベクター(AAVベクター)は増殖/非増殖のいずれの細胞にも遺伝子導入が可能であり、特に非分裂細胞においては長期間の目的遺伝子発現が可能です。アデノウイルスベクターやレトロウイルスベクターと比較して、免疫原性が低く、動物個体への遺伝子導入にも適しています。また、非病原性ウイルスであるため、P1レベルの施設でも取扱いが可能であり、安全で取扱いの容易なウイルスベクターとして広く使用されています*。
タカラバイオでは独自の技術を施した血清型1、2、5、6、8、9のAAV作製キット(AAVpro Helper Free System)、コントロールベクター作製キット、shRNA発現AAV作製キット、精製キット(AAVpro Purification Kit Maxi/Midi (All Serotypes)、またはAAVpro Purification Kit (AAV2))または、リアルタイムPCR法によるタイタ―測定キット(AAVpro Titration Kit (for Real Time PCR) Ver.2)などをご提供しています。
またウイルスを大量作製する場合に便利な高容量、高純度のパッケージングプラスミド(AAVpro Packaging Plasmid)を別売り製品としてご用意しています。
* 導入する目的遺伝子によっては、よりレベルの高い設備が必要です。
AAVの血清型について:
AAVには100を超える血清型が存在しており、血清型の違いによって宿主域やウイルスの持つ特徴が異なることが知られています。血清型2(AAV2)は古くから広く研究されてきた血清型の1つであり、宿主域が大変広いことが知られています。血清型1(AAV1)、血清型5(AAV5)、血清型6(AAV6)、血清型8(AAV8)と血清型9(AAV9)は、より高い組織指向性を持った血清型です。AAV1は筋肉、肝臓、気道、中枢神経系等、AAV5は中枢神経系、肝臓、網膜等、AAV6は心臓、筋肉、肝臓等、AAV8は肝臓、筋肉、中枢神経系等、AAV9は中枢神経系、心臓、肝臓、筋肉等への遺伝子導入効率が高いと言われています。
タカラバイオでは独自の技術を施した血清型1、2、5、6、8、9のAAV作製キット(AAVpro Helper Free System)、コントロールベクター作製キット、shRNA発現AAV作製キット、精製キット(AAVpro Purification Kit Maxi/Midi (All Serotypes)、またはAAVpro Purification Kit (AAV2))または、リアルタイムPCR法によるタイタ―測定キット(AAVpro Titration Kit (for Real Time PCR) Ver.2)などをご提供しています。
またウイルスを大量作製する場合に便利な高容量、高純度のパッケージングプラスミド(AAVpro Packaging Plasmid)を別売り製品としてご用意しています。
* 導入する目的遺伝子によっては、よりレベルの高い設備が必要です。
AAVの血清型について:
AAVには100を超える血清型が存在しており、血清型の違いによって宿主域やウイルスの持つ特徴が異なることが知られています。血清型2(AAV2)は古くから広く研究されてきた血清型の1つであり、宿主域が大変広いことが知られています。血清型1(AAV1)、血清型5(AAV5)、血清型6(AAV6)、血清型8(AAV8)と血清型9(AAV9)は、より高い組織指向性を持った血清型です。AAV1は筋肉、肝臓、気道、中枢神経系等、AAV5は中枢神経系、肝臓、網膜等、AAV6は心臓、筋肉、肝臓等、AAV8は肝臓、筋肉、中枢神経系等、AAV9は中枢神経系、心臓、肝臓、筋肉等への遺伝子導入効率が高いと言われています。
ワークフロー
|
Step 1:目的遺伝子のクローニング*1
|
*1 標的の細胞種、組織部位にあわせて血清タイプ(AAV1、AAV2、AAV5、AAV6、AAV8、AAV9)をご選択ください。 |

|
|
|
Step 2:ウイルスのパッケージング
|
|

|
|
|
Step 3:ウイルスの抽出
|
|

|
|
|
Step 4:ウイルスの精製*2
*2 動物個体へ遺伝子導入を行う際は、高純度に精製したウイルスベクターを使用 |
|

|
|
|
Step 5:ウイルスのタイタ―測定 |
|

|
|
|
Step 6:標的細胞、動物への遺伝子導入
|
Step 1:目的遺伝子のクローニング
AAVpro Helper Free System(製品コード 6673、6230、6650、6651、6680、6690)に含まれているpAAV-CMV Vectorに目的遺伝子をクローニングする。
目的遺伝子サイズは2.5 kb以内とする。
※標的の細胞種、組織部位にあわせて血清タイプをご選択ください。また、shRNA発現AAV作製用キットもご用意しています。
目的遺伝子サイズは2.5 kb以内とする。
※標的の細胞種、組織部位にあわせて血清タイプをご選択ください。また、shRNA発現AAV作製用キットもご用意しています。
Step 2:ウイルスのパッケージング
AAVpro Helper Free Systemにより、ヘルパーウイルスを使用せずにAAVベクターを作製する。目的遺伝子をクローニングしたpAAV-CMV Vectorとキットに含まれるpRC Vector、pHelper Vector*をAAVpro 293T Cell Line(製品コード 632273)にトランスフェクションして2~3日培養する。(AAV-2ベクターはpRC2-mi342 Vectorに搭載したhsa-miR-342により、高力価ウイルスを作製できる。)
* 動物個体への遺伝子導入など大量のウイルスを作製するのに便利なReady-to-Useの高容量トランスフェクション用プラスミドAAVpro Packaging Plasmidの別売り製品も用意しています。AAVpro Packaging Plasmidには、臨床開発での使用を想定した、カナマイシン耐性遺伝子を搭載したAAVベクター高容量プラスミドセット(AAV2、AAV6、AAV8、AAV9)もラインナップしています。
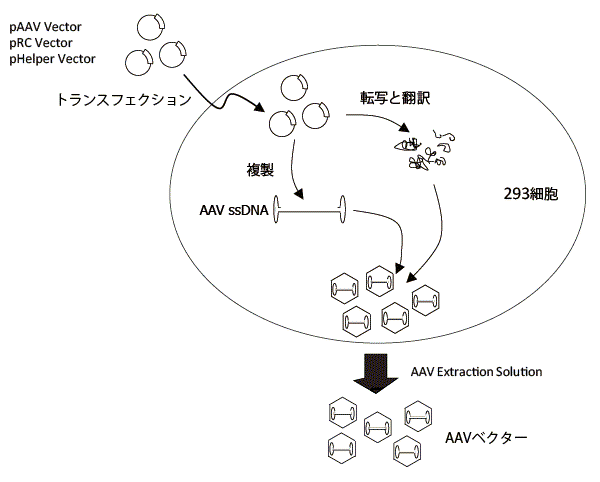
図. AAVpro Helper Free SystemによるAAV2ベクター作製
* 動物個体への遺伝子導入など大量のウイルスを作製するのに便利なReady-to-Useの高容量トランスフェクション用プラスミドAAVpro Packaging Plasmidの別売り製品も用意しています。AAVpro Packaging Plasmidには、臨床開発での使用を想定した、カナマイシン耐性遺伝子を搭載したAAVベクター高容量プラスミドセット(AAV2、AAV6、AAV8、AAV9)もラインナップしています。

図. AAVpro Helper Free SystemによるAAV2ベクター作製
Step 3:ウイルスの抽出
トランスフェクション後2~3日培養したAAVベクター産生細胞から、抽出試薬AAVpro Extraction Solution*を用いてAAVベクターの抽出を行う。
タカラバイオ独自のAAVベクター抽出法(特許出願中)により、凍結融解や超音波破砕などの面倒な操作は一切不要である。
* 抽出試薬AAVpro Extraction SolutionはAAVpro Helper Free System、AAVpro Purification Kit (AAV2)、AAVpro Titration Kit (for Real time PCR) に添付しています。また、さまざまな血清型のAAVベクターに使用することができるため、AAVpro Extraction Solution(製品コード 6235)として単品販売もしています。
タカラバイオ独自のAAVベクター抽出法(特許出願中)により、凍結融解や超音波破砕などの面倒な操作は一切不要である。
* 抽出試薬AAVpro Extraction SolutionはAAVpro Helper Free System、AAVpro Purification Kit (AAV2)、AAVpro Titration Kit (for Real time PCR) に添付しています。また、さまざまな血清型のAAVベクターに使用することができるため、AAVpro Extraction Solution(製品コード 6235)として単品販売もしています。
Step 4:ウイルスの精製
AAVpro Purification Kit Maxi/Midi (All Serotypes)(製品コード6666/6675)やAAVpro Cell & Sup. Purification Kit Maxi (All Serotypes)(製品コード 6676)、AAVpro Freeze-Thaw Extraction Buffer (All Serotypes) (製品コード 6679)を用いて組換えAAVベクターを高純度かつ高収率に精製することができる。本キットにより精製されたウイルスは、宿主細胞由来のタンパク質や核酸の混入が抑えられている。
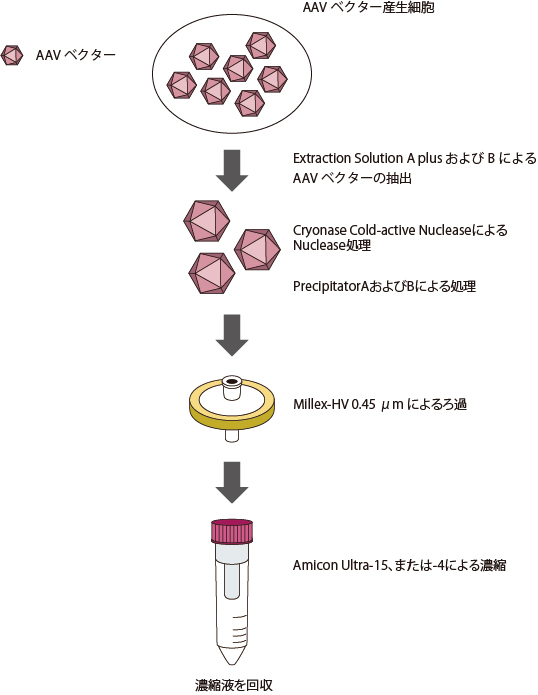
※AAVpro Purification Kit (AAV2)(製品コード 6232)を用いて組換えAAVベクターを精製することもできる。

※AAVpro Purification Kit (AAV2)(製品コード 6232)を用いて組換えAAVベクターを精製することもできる。
Step 5:ウイルスのタイター測定
AAVベクターのタイタ―測定は従来DNAブロット法やELISA法で行われているが、AAVpro Titration Kit (for Real Time PCR) Ver.2(製品コード 6233)はリアルタイムPCR法によりウイルスDNA量を高精度かつ短時間で測定できる。AAVウイルスの両末端にあるITR(Inverted Terminal Repeat)をターゲット配列としてウイルスゲノムを検出するため、幅広いAAVベクターの力価測定が可能である*。
* 本製品により測定可能なAAVベクターについて
AAVベクターの血清型は、ウイルス作製時に使用するpRCベクターにコードされているCap遺伝子の種類によって決定される。一方、AAV粒子内に封入されるベクターゲノムは、一般的には血清型に関わらず、共通してAAV2のITRが使用されている。本製品はAAV2由来のITRをターゲットとしてベクターゲノムを定量するキットであるため、ウイルス粒子内のベクターゲノムのITR領域がAAV2由来であれば、血清型に関わらず測定可能である。
* 本製品により測定可能なAAVベクターについて
AAVベクターの血清型は、ウイルス作製時に使用するpRCベクターにコードされているCap遺伝子の種類によって決定される。一方、AAV粒子内に封入されるベクターゲノムは、一般的には血清型に関わらず、共通してAAV2のITRが使用されている。本製品はAAV2由来のITRをターゲットとしてベクターゲノムを定量するキットであるため、ウイルス粒子内のベクターゲノムのITR領域がAAV2由来であれば、血清型に関わらず測定可能である。
Step 6:標的細胞、動物への遺伝子導入
アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入 文献情報
アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入に関する文献情報を以下のリンクよりご覧いただけます。
実験条件による遺伝子導入効率の程度や、実験目的に合った血清型の選択にお役立て下さい。
文献情報まとめサイト『アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入 参考文献』の掲載内容
実験条件による遺伝子導入効率の程度や、実験目的に合った血清型の選択にお役立て下さい。
文献情報まとめサイト『アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入 参考文献』の掲載内容
製品ラインナップ
| 用途 | 製品名 |
|---|---|
| AAV作製用キット | AAVpro Helper Free System(製品コード 6230)他 |
| shRNA発現AAV作製用キット | AAVpro Helper Free System (AAV-2xU6)(製品コード 6661)他 |
| AAV大量作製用パッケージングプラスミド | AAVpro Packaging Plasmid(製品コード 6234)他 |
| コントロールベクター | AAVpro Helper Free System(AAV-LacZ)(製品コード 6655)、 AAVpro Helper Free System(AAV-CRE Recombinase)(製品コード 6652)他 pAAV-ZsGreen1 Vector (製品コード 6231、6610) |
| AAVパッケージング用細胞 | AAVpro 293T Cell Line(製品コード 632237) |
| AAV2精製キット(AAV2専用) | AAVpro Purification Kit (AAV2)(製品コード 6232) |
| AAV精製キット(様々な血清型に適用可能) | AAVpro Purification Kit Maxi/Midi (All Serotypes)(製品コード 6666/6675) |
| qPCRタイタ―キット | AAVpro Titration Kit (for Real Time PCR) Ver.2(製品コード 6233) |
| AAV抽出試薬 | AAVpro Extraction Solution(製品コード 6235) |
| AAVベクタータイプのTet-One発現誘導システム | AAVpro Tet-One Inducible Expression System (AAV2)(製品コード 634310) |
注:AAVpro Helper Free System、AAVpro Purification Kitおよび製品コード 6233、634310にはAAVpro Extraction Solutionが含まれている。
関連資料
関連のオンラインガイドはこちら
Application
AAV2ベクターを用いたマウス脳線条体への遺伝子導入
【参考データ】pRC2-mi342 Vector使用によるAAV2ベクタータイター向上効果
【参考データ】AAV Extraction SolutionによるAAV2ベクター抽出効果
Technical Notes
組換えウイルス発現系選択ガイド
アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入 参考文献
関連製品・受託
Tet-One™発現誘導システム
AAVpro® Purification Kit (AAV2)
AAV qPCR(リアルタイムPCR)迅速タイター測定キット
AAVpro® 293T Cell Line
AAVpro® Helper Free System
AAVpro® Extraction Solution
pAAV-ZsGreen1 Vector
CalPhos™ 哺乳類細胞用トランスフェクション試薬
TransIT®-293 Reagent
Xfect™ トランスフェクション試薬
EDTA Buffer Powder
アデノ随伴ウイルス(AAV)ベクター作製
この製品を見た人は、
こんな製品も見ています
-
アデノ随伴ウイルス(AAV)ベクターによる遺伝子導入 参考文献
-
AAVpro® Purification Kit Maxi/Midi (All Serotypes)
様々な血清型アデノ随伴ウイルスベクターに適用できる高効率な精製キット
-
pAAV-ZsGreen1 Vector
蛍光タンパク質搭載AAVベクター
-
AAVpro® Helper Free System
ヘルパーフリーシステムによるAAVベクターの作製
-

AAV qPCR(リアルタイムPCR)迅速タイター測定キット
様々なアデノ随伴ウイルス(AAV)ベクターの力価測定が可能
-

AAVpro® Purification Kit (AAV2)
高純度かつ簡便にAAV2を精製
- 注意事項
- 本ページの製品はすべて研究用として販売しております。ヒト、動物への医療、臨床診断用には使用しないようご注意ください。また、食品、化粧品、家庭用品等として使用しないでください。
- タカラバイオの承認を得ずに製品の再販・譲渡、再販・譲渡のための改変、商用製品の製造に使用することは禁止されています。
- タカラバイオ製品に関連するライセンス・パテントについては、ライセンスマークをクリックして内容をご確認ください。
また、他メーカーの製品に関するライセンス・パテントについては、各メーカーのウェブサイトまたはメーカー発行のカタログ等でご確認ください。 - ウェブサイトに掲載している会社名および商品名などは、各社の商号、または登録済みもしくは未登録の商標であり、これらは各所有者に帰属します。


